Физические свойства
Строение 1. Причина кислотности- крайний водород, способный к замещению 2. Эффект сопряжения сильнее, чем индуктивный Кислотные свойства 1. Чем меньше R, тем сильнее кислотные свойства 2. Галогены усиливают кислотные свойства 3. Чем ближе галоген к карбоксильной группе, тем сильнее кислота Номенклатура 1)HCOOH – Муравьиная (формиаты) 2)CH3COOH – Уксусная (ацетаты) 3)C2H5COOH – Пропионовая, пропановая 4)C3H7COOH – Масляная, бутановая 5)C4H9COOH – Валериановая, пентановая 6)C5H11COOH – Капроновая, гексановая 7) HOOCCOOH - Щавелевая кислота (двухосновная)(оксалат- соль) 8) НООС-СН2-СН2-СООН – Янтарная кислота 9)СН2=СН–СООН – Акриловая кислота(акрилат –соль) Высшие карбоновые кислоты C15H31COOH – Пальмитиновая, гексадекановая С17H35COOH – Стеариновая кислота С17H31COOH - Линолевая кислота(2+1) С17H29COOH – Линоленовая кислота(3+1) C17H33COOH – Олеиновая кислота(1+1) Изомерия
· Межклассовая (к-та = сложный эфир) Пространственная · Оптическая Получение 1) Жесткое окисление алкенов 2) Из альдегидов(+Ag2O,Cu2O аммиачн раствор, Cu(OH)2, KMnO4 H+) 3) Из спиртов(KMnO4 H+) 4) Из Алкинов и алкенов (KMnO4 H+) 5) Гидролиз сложных эфиров 6) CH3COONa + HCl → CH3COOH + NaCl Физические свойства 1) Жидкости с высокой температурой кипения, растворимы в H2O (из-за водородных связей) 2) C1-C3 резкий запах 3)
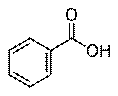
Бензойная кислота Терефталевая кислота Эфиры - органические вещества с эфирной связью. …-О-…
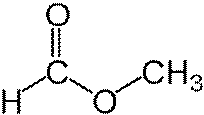
Диметиловый эфир Метил формиат
|


 С10 –твердое, без запаха, H2O
С10 –твердое, без запаха, H2O




 Простые Сложные
Простые Сложные