Оксид азота IV
Диоксид азота NO2 - газ бурового цвета, токсичен. Его молекула – парамагнитна, имеет угловую форму NO2 N2O4 Бурый Бесцветный парамагнитен диамагнитен Жидкий и твердый диоксид азота бесцветен, состоит из молекул N2O4. Молекула плоская, диамагнитная. Диоксид азота образуется при окислении NО, также при разложении нитратов тяжелых металлов: 2Рb(NO3)2=2РbO+4NO2+O2. В лаборатории NO2 получают при действии концентрированной азотной кислоты на медь Cu+4HNO3конц=Cu(NO3)2+2NO2+2H2O Оксид хорошо растворяется в воде 2NO2+H2O=HNO2+HNO3 HNO2+NO2=HNO3+NO 3NO2+H2O=2HNO3+NO. Растворение NO2 в воде при избытке кислорода под давлением идет по уравнению 2NO2+2H2O+O2=4HNO3. При растворения в щелочи также образуется смесь нитратов и нитритов:
1NO2 + Н2О – е = NO3ˉ + 2Н+ 1 NO2 + е = NO2ˉ NO2 + H2O + NO2 = NO3ˉ + 2Н+ +NO2ˉ
|

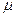 = 0,29 Д; <ONO=1320. Длина связи dNN равна 1,20 А°, т.е. имеет промежуточное значение между длиной одинарной (1,43 А) и двойной (1,18 А) связи, в соответствии с этим атому азота можно приписать sр2-гибридизацию валентных орбиталей. Так как в молекуле NO2 существует нечетное количество электронов (5+6 × 2=17), молекула легко димеризуется:
= 0,29 Д; <ONO=1320. Длина связи dNN равна 1,20 А°, т.е. имеет промежуточное значение между длиной одинарной (1,43 А) и двойной (1,18 А) связи, в соответствии с этим атому азота можно приписать sр2-гибридизацию валентных орбиталей. Так как в молекуле NO2 существует нечетное количество электронов (5+6 × 2=17), молекула легко димеризуется: 2NO2+KOH=KNO3+KNO2+H2O
2NO2+KOH=KNO3+KNO2+H2O


