Окисно-відновні реакції
Мета роботи: простежити за ходом окисно-відновних реакцій, скласти рівняння реакцій і зрівняти методом електронного балансу, визначити окисник та відновник. Дослід 1. У розчин купрум (II) сульфату опустіть на 3-5 хвилин залізний цвях, поверхня якого очищена наждаковим папером. Опишіть спостереження в ході реакції. Складіть рівняння реакції і зрівняйте методом електронного балансу. ____________________________________________________________________________________________________________________________________________ Дослід 2. До 2 крапель розчину калій йодиду долийте 2 краплі розчину сульфатної кислоти Н2SО4 і 2 краплі розчину калій йодату КIО3. Опишіть спостереження в ході реакції. Складіть рівняння реакції і зрівняйте методом електронного балансу. Доведіть наявність вільного йоду за взаємодією з крохмалем. ____________________________________________________________________________________________________________________________________________ Дослід 3. До 2 крапель розчину калій дихромату К2Сr2О7 додайте 2 краплі розведеної сульфатної кислоти і 2 краплі розчину калій нітриту КNO2. Опишіть спостереження в ході реакції. Складіть рівняння реакції і зрівняйте методом електронного балансу. ____________________________________________________________________________________________________________________________________________ Дослід 4. У 3 пробірки налийте по 1 краплі розчину калій перманганату КМnО4. У першу пробірку додайте 2-3 краплі розчину сульфатної кислоти, у другу – дистильованої води, у третю – 4 краплі розчину натрій гідроксиду. В усі пробірки додайте кристалічний натрій сульфіт. Опишіть спостереження в ході реакцій. Складіть рівняння реакцій і зрівняйте методом електронного балансу. ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ ____________________________________________________________________________________________________________________________________________ Дослід 5. Визначення напрямку окисно-відновної реакції: Сr(NО3)3 + К2SО4 + I2 + H2O = К2Сr2О7 + КI + Н2SО4 + КNО3. а) Внесіть в пробірку по 2 краплі хром (III) нітрату, калій сульфату і додайте до них 1-2 краплі розчину йоду. Чи відбувається окиснення хрому (III) йодом, що повинно супроводжуватися знебарвленням йоду? б) Внесіть в пробірку по декілька крапель розчину калій дихромату і сульфатної кислоти, потім додайте 3-4 краплі калій йодиду. Опишіть спостереження в ході реакцій. Визначте, у прямому чи зворотному напрямку протікає окисно-відновна реакція? ____________________________________________________________________________________________________________________________________________ Завдання для самоконтролю до теми "Окисно-відновні реакції"; 1. Які реакції називаються окисно-відновними? 2. Вкажіть типи окисно-відновних реакцій. 3. Які речовини в окисно-відновних реакціях називаються відновниками, а які – окисниками? 4. Визначте ступінь окиснення Сr в наступних сполуках: К2СrО4, Сr2О3, Fе(СrО2)2, К2Сr2О7, Сr2(SО4)3. 5. Вкажіть, які із приведених процесів являють собою окиснення, а які – відновлення: S → SO 6. Дорівняйте реакції методом електронного балансу. До якого типу окисно-відновних реакцій відносяться рівняння? а) КМnО4 + КОН → К2МnО4 + О2 + Н2О; б) NН4NО2 → N2 + Н2О; в) NаОН + S → Nа2S + Nа2SО3 + Н2О; г) Р + КОН + Н2О → РН3 + КН2РО2; д) Н2О2 → О2 + Н2О; є) КМnО4 + МnSО4 + Н2О → МnО2 + К2SО4 + Н2SО4; е) Zn + HNO3 → Zn(NO3)2 + N2O + H2O; ж) NH4NO3 → N2O + H2O; з) H2S + HNO3 → S + NO2 + H2O; і) Аg + HNO3 → AgNO3 + NO2 + H2O. 7. Закінчіть і зрівняйте рівняння реакцій, вкажіть окисник і відновник: а) Мn(ОН)2 + Сl2 + КОН → МnО2 +... б) МnО2 + О2 + КОН → К2МnО4 +... в) РbS + НNО3 → РbSО4 + NО2 +... г) КМnО4 + FeSО4 + Н2SО4 → д) К2Cr2О7 + НCl → е) Н2S + К2Cr2О7+ Н2SО4 →.
|

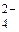 ; S → S
; S → S  ; Sn → Sn
; Sn → Sn  ; К → К+; Вr2 → 2Вr
; К → К+; Вr2 → 2Вr 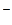 ; 2Н+ → Н2; Н2 → 2Н–; СI– → СIО
; 2Н+ → Н2; Н2 → 2Н–; СI– → СIО 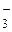 ; V2+ → VO3–; IО
; V2+ → VO3–; IО  → МnО
→ МnО 


