ДАЛЬНИЕ КОНСТАНТЫ ССВ В ПРОИЗВОДНЫХ ПИРАЗОЛО[1,5-A]ПИРИМИДИНА КАК КРИТЕРИЙ ОТНЕСЕНИЯ РЕГИОИЗОМЕРОВ
Ломовская М.И.,1 Касаточкин А.Н.2
1 Санкт-Петербургский государственный университет, Санкт-Петербург, Россия. Студент VI курса. Marijaregina@mail.ru 2 Санкт-Петербургский государственный университет, Санкт-Петербург, Россия. Молодой учёный. Научный руководитель: С.И.Селиванов, А.А.Петров
Производные пиразоло[1,5-a]пиримидина являются важным классом гетероциклических соединений, обладающих широким спектром физиологической активности, которая зависит от природы и положения заместителей в молекуле. При синтезе замещенных пиразоло[1,5-a]пиримидинов возможно образование изомерных соединений в результате конкурентной атаки нуклеофильных центров 3(5)-аминопиразола (NH2, N1). Ранее было показано, что для производных пиразоло[1,5-a]пиримидина в качестве критерия отнесения региоизомеров можно использовать как ХС атомов углерода пиримидинового кольца, так и ХС протонов и атомов углерода заместителей в пиримидиновом кольце [1-3]. В настоящей работе с целью получения дополнительных прямых критериев региостроения производных пиразоло[1,5-a]пиримидина измерены дальние КССВ 5J(H,H), 4J(H,Н), 3J(С,Н), 5J(H,F), 4J(H,F) и 3J(С,F). По данным спектров ЯМР 1Н в пиразоло[1,5-a]пиримидине 1 между протонами метильной группы 7-СН3 и протоном Н(6) наблюдается КССВ 4J(H,H) ~ 1.0 Гц, но не наблюдается КССВ между 5-СН3 и протоном Н(6). В общем случае величина 4J(H,F) больше соответствующей КССВ между протонами, однако в соединении 2 величина4J(H,F) ~ 0 Гц. Электроноакцепторный заместитель СF3 уменьшает электронную плотность на атомах углерода двойной связи, через которые передается ССВ, что приводит к уменьшению КССВ 4J(H,F) по сравнению с 4J(H,H). В то же время в спектрах ЯМР 13С обоих соединениях наблюдаются по две 3J (C,H), 4J (C,H) и 3J (C,F), но их значения отличаются в два и более раз (схема). В трициклических соединениях 3, 5, 7 между метиленовыми протонами 6-СН2 и 8(9)-СН2 циклоалкенового кольца наблюдаются КССВ 5J(H,H) ~ 1.5 Гц, в региоизомерных структурах 4, 6 КССВ 5J(H,H) между метиленовыми протонами 5-СН2 и 7(8)-СН2 циклоалканового кольца не наблюдается. В производных пиразолопиримидина, аннелированных циклоалкенами (циклоалканами) 3-7, все формально простые связи C–C, C–N и N–N значительно короче по сравнению с типичными длинами связей (1.54, 1.47 and 1.45A˚ соответственно, что свидетельствует о значительной степени делокализации p- и n-электронов. Разница в длинах связей между псевдопростой и псевдодвойной связями С(5)-С(6) и С(6)=С(7) в пиразоло[1,5-a]пиримидинах и их аннелированных производных по данным РСА составляет приблизительно ~ 0.045-0.083 Ǻ. Передача ССВ по системе связей H–C6–C5а=C9а(8а)–C9(8)–H (соединения 3, 5, 7) значительно более эффективна, чем по системы связей H–C5–C4а–C8а(7a)–C8(7)–H, что определяется большей эффективностью передачи скалярных взаимодействий через двойную связь, чем через цепочку простых связей [1]. Аналогичные закономерности наблюдаются для трициклических соединений 8 и 9, содержащих трифторметильную группу. В этих структурах КССВ 5J(H,H) между метиленовыми протонами 5-СН2 и 7(8)-СН2 циклоалканового кольца не наблюдается, а КССВ 5J(H,F) между метиленовыми протонами 7(8)-СН2 и атомами фтора группы CF3 2.9 и 3.1 Гц соответственно. Следует отметить, что в соединениях 8 и 9 для КССВ 5J(H,F) нельзя исключить прямого магнитного взаимодействия ядер 1Н и 19F через пространство. При введении метильной группы в положение 7 циклогексенового кольца 6,7,8,9-тетрагидропиразоло[1,5-a]хиназолина 7, занимающей псевдоаксиальное положение, инверсия циклогексенового кольца заторможена, и наблюдаются три из четырех КССВ 5J(H,H) между метиленовыми протонами при атомах С(6) и С(9): 5 J (H6 a, H9 a) ~ 2.4 Гц, 5 J (H6 a, H9 e) ~ 1.4 Гц, 5 J (H9 a, H9 e) ~ 1.3 Гц, 5 J (H6 e, H9 e) <0.1 Гц.
МЕТОДЫ СИНТЕЗА НОВЫХ БИС-ИМИДОФЕНОКСИТЕТРАКАРБОНОВЫХ КИСЛОТ (МОНОМЕРОВ А2-ТИПА)МЕТОДЫ СИНТЕЗА НОВЫХ БИС-ИМИДОФЕНОКСИ-ТЕТРАКАРБОНОВЫХ КИСЛОТ (МОНОМЕРОВ А2-ТИПА)
Луференко Д.В.,1 Доброхотов О.В.2,Чиркова Ж.В.3
1 ФГБОУ ВПО "Ярославский Государственный Технический Университет", Ярославль, Россия. Студент II курса. LuferenkoD@mail.ru 2 ФГБОУ ВПО "Ярославский Государственный Технический Университет", Ярославль, Россия. Аспирант 1г. 3 ФГБОУ ВПО "Ярославский Государственный Технический Университет", Ярославль, Россия. Молодой учёный. Научный руководитель: Абрамов И.Г.
В современных высокотехнологичных областях науки и техники, таких как аэрокосмический комплекс, атомная энергетика, транспортное машиностроение, электроника, электротехника и т.п. необходимы материалы, обладающие высокой термической, криогенной и радиационной стойкостью, а также высокими прочностными показателями в большом температурном диапазоне. Указанным требованиям отвечают полиимидные (ПИ) материалы.
Нами разработаны методы синтеза и технология получения новых бисимидофенокситетракарбоновых кислот (мономеров А2-типа). Для этого использовались доступные диангидриды 1 (а-с), которые конденсировали с аминофеноксифталевой кислотой 2 в соотношении 1:2, соответственно. Синтез аминофеноксифталевой кислотой 2 разработан нами ранее [1]. Варьируя исходные реагенты, мы получили новые производные тетракарбоновых кислот 3 (а-с), строение которых подтверждено спектральными данными.
Литература: [1]. Кузнецов А.А., Бузин П.В., Яблокова М.Ю., Смирнов А.В. Абрамов И.Г. Патент РФ № 2259352.
|

 ЯМР 1Н:
H6 (к), 7-СH3 (д), 5-СH3 (с)
4J (7–СH3–H6) ~ 1.0 Гц
ЯМР 13С:
5-СН3 и 7-СН3 (д.к),
3J (7–СH3–Н6) 3.7 Гц,
3J (5–СH3–H6) 1.8 Гц
ЯМР 1Н:
H6 (к), 7-СH3 (д), 5-СH3 (с)
4J (7–СH3–H6) ~ 1.0 Гц
ЯМР 13С:
5-СН3 и 7-СН3 (д.к),
3J (7–СH3–Н6) 3.7 Гц,
3J (5–СH3–H6) 1.8 Гц
 ЯМР 1Н:
H6 (с),
ЯМР 13С:
5-СF3 и 7-СF3 (к.д),
4J (7–СF3–Н6) 4.1 Гц,
4J (5–СF3–H6) 1.4 Гц
C6 (к.к),
3J (7–СF3–С6) 4.2 Гц,
3J (5–СF3–С6) 2.1 Гц
ЯМР 1Н:
H6 (с),
ЯМР 13С:
5-СF3 и 7-СF3 (к.д),
4J (7–СF3–Н6) 4.1 Гц,
4J (5–СF3–H6) 1.4 Гц
C6 (к.к),
3J (7–СF3–С6) 4.2 Гц,
3J (5–СF3–С6) 2.1 Гц
 ЯМР 1Н:
6-СH2 (т.т), 9-СH2 (т.т),
5J (9-CH2, 6-CH2) 1.6 Гц
ЯМР 1Н:
6-СH2 (т.т), 9-СH2 (т.т),
5J (9-CH2, 6-CH2) 1.6 Гц
 ЯМР 1Н:
9-СH3 (уширен),
J (8-CH2, 9-CH3) < 0.5 Гц
ЯМР 1Н:
9-СH3 (уширен),
J (8-CH2, 9-CH3) < 0.5 Гц
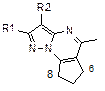 ЯМР 1Н:
6-СH2 (т.т), 8-СH2 (т.т),
5J (6-CH2, 8-CH2) 1.4 Гц
ЯМР 1Н:
6-СH2 (т.т), 8-СH2 (т.т),
5J (6-CH2, 8-CH2) 1.4 Гц
 ЯМР 1Н:
7-СH2 (т.к), 8-СH3 (т),
5J (7-CH2, 8-CH3) 1.1 Гц
ЯМР 1Н:
7-СH2 (т.к), 8-СH3 (т),
5J (7-CH2, 8-CH3) 1.1 Гц
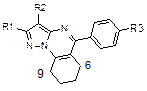 ЯМР 1Н:
6-СH2 (т.т), 9-СH2 (т.т),
5J (9-CH2, 6-CH2) ~ 1.6 Гц
ЯМР 1Н:
6-СH2 (т.т), 9-СH2 (т.т),
5J (9-CH2, 6-CH2) ~ 1.6 Гц
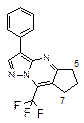 ЯМР 1Н:
H7(т.к),
5J (8–СF3–Н7) 2.9 Гц
ЯМР 13С: [4]
С7 (т.к),
4J (8–СF3–С7) 2.7 Гц
ЯМР 1Н:
H7(т.к),
5J (8–СF3–Н7) 2.9 Гц
ЯМР 13С: [4]
С7 (т.к),
4J (8–СF3–С7) 2.7 Гц
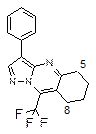 ЯМР 1Н:
H8 (т.к),
5J (9–СF3–Н8) 3.1 Гц
ЯМР 13С: [4]
С8 (т.к),
4J (9–СF3–С8) 3.3 Гц
ЯМР 1Н:
H8 (т.к),
5J (9–СF3–Н8) 3.1 Гц
ЯМР 13С: [4]
С8 (т.к),
4J (9–СF3–С8) 3.3 Гц




