РЕГИОСЕЛЕКТИВНОСТЬ 1,3-ДИПОЛЯРНОГО ЦИКЛОПРИСОЕДИНЕНИЯ НИТРОНОВ К АЛЛЕНАМ
Малинина Ю.В.
Санкт-Петербургский государственный университет, Санкт-Петербург, Россия. Студент III курса. cinse@mail.ru Научный руководитель: д.х.н., проф. Молчанов А.П.
1,3-Диполярное циклоприсоединение является одним из наиболее удобных методов для создания N,O-содержащих гетероциклических систем. Соединения ряда изоксазолидина имеют большое значение в связи с их потенциальной биологической активностью, кроме того они являются предшественниками 1,3-аминоспиртов, и, следовательно, антибиотиков и алкалоидов, содержащих β-лактамный цикл. Нами исследованы реакции 1,3-диполярного циклоприсоединения С-амидо и С,С-диметоксикарбонилнитронов к алленам, которые протекают регио- и стереоселективно с хорошим выходом, с образованием соответствующих изоксазолидинов. В данной работе установлено, что при комнатной температуре, в бензоле, циклоприсоединение алленов к С-амидо нитронам происходит по более замещённой двойной связи, с образованием только 4-метилен изоксазолидинов в виде двух диастереомеров в соотношении 11:1.
Таблица 1.
Региоселективность циклоприсоединения установлена на основании спектров ПМР реакционных смесей. Стереохимия продуктов была установлена с помощью NOESY 1H спектров для соединений 3b и 4b. В NOESY 1H спектрах соединений наблюдается взаимодействие протона Н1 N-ароматического кольца с протонами изоксазолидинового кольца Н2 и Н3 для соединений 3, а для соединений типа 4 наблюдается взаимодействие протона Н1 N-ароматического кольца с протоном изоксазолидинового кольца Н3, а взаимодействия с протоном Н2 не наблюдается.
При взаимодействии С,С-диметоксикорбонилнитронов в бензоле, при нагревании, с алленами получаются продукты изомеризации образующихся 5-метиленизоксозолидинов. То есть, в образующихся изоксазолидинах идёт раскрытие N-O связи с образованием циклоаддуктов(7, 8 и 9).
Из таблиц видно, что С-амидо нитроны обладают большей реакционной способностью, чем С,С-диметоксикорбонил нитроны.
Литература: [1]. Avijit B., Piyali S., Indian Inst. Sci., Recent studies on 1,3-dipolar cycloadditions of nitrone, 81, 313–323(2001). [2]. Krause N., Stephen A., Hashmi K., Modern allene chemistry(2004). [3]. R. C. F. Jones, J. N. Martin, A. Padwa, W. H. Pearson, Synthetic Application of 1-3-Dipolar Cycloaddition Chemistry Toward Heterocycles and Natural Products, Wiley, New Yok, 1 (2002). [4]. J. J. Tufariello, A. Padwa, 1,3-Dipolar Cycloaddition Chemistry, Wiley, New York, Vol. 2, 83(1984).
|

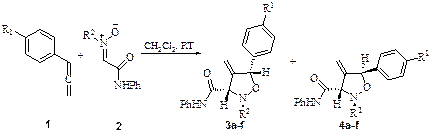

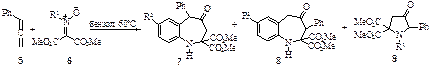 Таблица 2.
Таблица 2.


