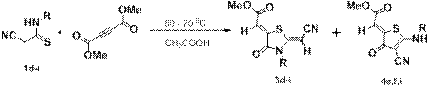СИНТЕЗ ТИОФЕНОВ ИЗ N-ЗАМЕЩЕННЫХ ТИОАЦЕТАМИДОВ
Обыденнов К.Л.
Уральский федеральный университет, Екатеринбург, Россия. Аспирант 1г. obydennovkl@e1.ru Научный руководитель: Моржерин Ю.Ю.
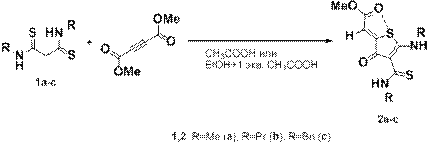
Химия азот- и серусодержащих гетероциклов в течение нескольких последних десятилетий остается одной из интенсивно развивающихся областей направленного органического синтеза. Это связано как с биологической активностью этих соединений, так и различными уникальными физико-химическими свойствами. Особый интерес в этом классе веществ представляют оксотиазолидины и тиофены, содержащие экзоциклические двойные С=С связи. Одним из способов получения гетероциклов, содержащих экзоциклические связи, является реакция между ацетилендикарбоксилатами и тиоацемидами. Ранее нами было показано, что в мягких условиях в спирте или хлористом метилене гетероциклизация тиоамидов под действием эфиров ацетилендикарбоновой кислоты происходит с образованием - 4-оксотиазолидин-2,5-илиденов [1, 2, 3]. Как оказалось, N,N`-дизамещенные малондитиоамиды 1a-c с метиловым эфиром ацетилендикарбоновой кислоты в уксусной кислоте взаимодействуют с образованием 3-оксотиофенов 2a-c. В спектрах ЯМР Н1 соединений 2a-c в области, характерной для СН= протонов, мы наблюдали только один сигнал. Структура соединения 2a была подтверждена данными рентгено-структурного анализа.
В то же время, в условиях уксусной кислоты в присутствии хлорной метилпропиолат [4] и фенилацетиленкетон [5],[6] взаимодействуют с малондитиоамидами с образованием дитиинового цикла. Взаимодействие N`-замещенных циантиоацетамидов 1d-i с диметиловым эфиром ацетилендикарбоновой кислоты как в спирте, так и в уксусной кислоте приводит к образованию либо смеси 4-оксотиазолидин-2,5-илиденовов 3d-i и 3-оксотиофен-2-илиденов 4e,f,i, либо только к производным тиазола.
Образование тиофенов в аналогичной реакции происходит в случае N,N-дизамещенных циантиоацетамидов [7]. Таким образом, нами была изучены некоторые факторы, влияющие на направление реакции гетероциклизации тиоацетамидов с метиловым эфиром ацетилендикарбоновой кислоты.
Литература [1]Berseneva V.S., Tkachev A.V., Morzherin Yu.Yu., Dehaen W., Luyten I., Toppet S., Bakulev V.A.,J. Chem. Soc. Perkin Trans., 1,2133 – 2136 (1998) [2]Bakulev V.A., Berseneva V.S., Belskaia N.P., Morzherin Yu.Yu., Zaitsev A., Dehaen W., Luyten I., Toppet S., Org.&Biomol. Chem., 1, 134-139 (2003) [3]Obydennov K.L., Kosterina M.F., Klimareva E.L., Bakulev V.A., Morzherin Yu.Yu., Russian Chemical Bulletin, 5, 1016-1018 (2011) [4]Волкова К.А., Нахманович А.С., Елохина В.Н., Ярошенко Т.И., Ларина Л.И., Шулунова А.М., Амосова С.В, Журнал органической химии, 5. 768-770 (2007) [5]Елохина В.Н., Ярошенко T.И., Нахманович A.С., Ларина Л.И., Амосова, Журнал органической химии 2006, 12, 1916-1918 (2006) [6]Низовцева Т.В., Комарова Т.Н., Нахманович А.С., Ларина Л.И., Лопырев В.А., Калистратова Е.Ф. Журнал органической химии, 8, 1205-1207, (2002) [7]Kosterina M.F., Morzherin Yu.Yu., Tkachev A.V., Rybalova T.V., Gatilov Yu.V., Bakulev V.A.,Russian Chemical Bulletin, 4, 613-618 (2002)
|