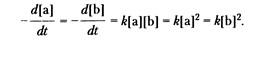Кинетика поликонденсации.
Протекание поликонденсации во времени может быть выражено изменением количества или концентраций реагентов - функциональных групп или мономеров, а также изменением во времени степени полимеризации образующихся макромолекул. Если реакционная способность всех реагентов (мономеров или олигомеров) одинакова, то поликонденсацию можно рассматривать как одну химическую реакцию. Наиболее простым случаем является поликонденсация мономеров типа а-а, например:
Для этой бимолекулярной реакции, если принебречь ее обратимостью на начальной стадии, скорость расходования функциональных групп описывается простым кинетическим уравнением для реакции второго порядка:
Это уравнение, естественно, пригодно для описания во времени гетерополиконденсации мономеров а-а и b-b при их исходном эквимольном соотношении в реакционной смеси. Скорость поликонденсации можно выразить также через изменение концентрации мономера. Для бифункциональных мономеров (для начальных стадий процесса пока в реакционной смеси имеются только мономер и димеры)
т. е. скорость убыли мономера вдвое больше скорости расходования функциональных групп. При поликонденсации мономеров с зависимыми функциональными группами, в которых активность второй группы изменяется после вступления первой в полимерную цепь, проходится учитывать реакционную способность второй (вторичной) функциональной группы н рассматривать поликонденсацию как последовательную реакцию, в которой происходит убыль одних функциональных групп и появление других (иной реакционной способности). Дифференциальные уравнения изменения концентрации функциональных групп для таких мономеров имеют вид:
|