Розділ 5
Окисно–відновні реакції (ОВР)
Еталони розв’язання типових задач Завдання. Закінчити рівняння реакцій. а) Cl
б) Pb+4O2 + 2KI– + 2H2SO4 " Pb+2SO4 + I
в) 3Fe+2O + 10HN+5O3 " 3Fe+3(NO3)3 + N+2O + 5H2O
г) 2KMn+7O4 + 5KN+3O2 + 3H2SO4 " 2Mn+2SO4 + 5KN+5O3 + K2SO4 + 3H2O
Скорочуємо на „3”: 2Ag+1N+5O
Розділ 6 Комплексні сполуки
Еталони розв’язання типових задач Приклади тестового контролю: 5.1. Назвіть комплексну сполуку [Cu(NH3)4]SO4: а) сульфаттетрааміак міді (ІІ); б) сульфаттетрамін міді (ІІ); в) мідісульфатетрамін (ІІ). 5.2. Напишіть формулу іонізаційного ізомеру сполуки [Co(H2O)5]Cl3: а) [CoCl3]. [H2O]5; б) [Co(H2O)5Cl]Cl2; в) [Co(H2O)3]Cl3.2H2O. 5.3. Визначте заряд комплексного іону в сполуці [Cr(H2O)4Cl2]Cl.2H2O: а) 4+; б) 2+; в) 3+. 5.4. Напишіть формулу загальної Кнест. комплексного іону [NiCl4]2–: а) Kнест.= 5.5. Визначте заряд центрального іону в сполуці Fe2[Fe(CN)6]: а) 2+; б) 6+; в) 3+. 5.6. Напишіть формулу комплексної сполуки, якщо координаційне число становить чотири Zn(OH)2+2NaOH: а) [ZnNa2(OH)2](OH)2; б) Na2[Zn(OH)4]; в) Zn[Na2(OH)4]. 5.7. Напишіть продукти первинної дисоціації сполуки Na3[AlF6]: а) 3Na+ + [AlF6]3–; б) Na
ЛАБОРАТОРНИЙ ПРАКТИКУМ
ПРАВИЛА РОБОТИ І ТЕХНІКА БЕЗПЕКИ В ЛАБОРАТОРІЇ НЕОРГАНІЧНОЇ ХІМІЇ
|

 + 2NaOH " NaCl– + NaCl+O + H2O
+ 2NaOH " NaCl– + NaCl+O + H2O " Cl–
" Cl–
 + K2SO4 + 2H2O
+ K2SO4 + 2H2O д) 6Ag+1N+5O
д) 6Ag+1N+5O  " 6AgO + 6N+4O2h + 3O
" 6AgO + 6N+4O2h + 3O 
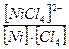 ; б) Kнест.=
; б) Kнест.=  ; в) Kнест.=
; в) Kнест.=  .
. + Al3+ + 6F–; в) 3Na+ + Al3+ + F
+ Al3+ + 6F–; в) 3Na+ + Al3+ + F  .
.


