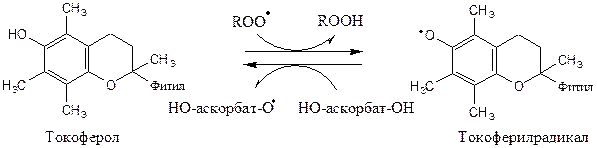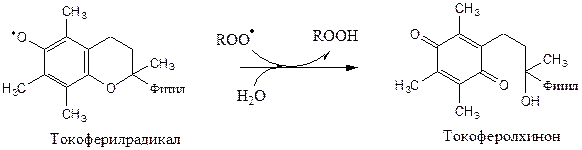Неферментативная антиоксидантная система
" Липидные антиоксиданты " - производные фенола, способны инактивировать свободные радикалы в гидрофобном слое мембран и предотвращать развитие ПОЛ. К ним относится α-токоферол (витамин Е), убихинон (коэнзим Q), тироксин и синтетические соединения, например ионол (бутилированный гидрокситолуол). Витамин Е (α-токоферол) самый распространённый липофильный антиоксидант, он обеспечивает защиту мембран от СРО. Различают 8 типов токоферолов, но α-токоферол наиболее активен. α-Токоферол отдаёт атом водорода радикалу липида ROO ∙, восстанавливает его до гидропероксида (ROOH), а сам превращается в малоактивный свободный радикал, что прерывает ПОЛ:
Регенерацию α-токоферола осуществляет витамин С. Свободный радикал витамина Е стабилен и не поддерживает ПОЛ, он взаимодействует с радикалами липидных перекисей, восстанавливает их, а сам превращается в стабильную окисленную форму — токоферолхинон.
Витамин С ингибирует СРО с помощью двух различных механизмов: 1). восстанавливает в мембранах токоферолхинон до витамина Е: НО-аскорбат-ОН + α-ТФ-О· → α-ТФ-ОН + НО-аскорбат-О· (семидегидроаскорбиновая к-та) НО-аскорбат-О· + α-ТФ-О· → α-ТФ-ОН + О=аскорбат=О (дегидроаскорбиновая к-та)
Регенерация аскорбиновой кислоты идет с участием ферментативных систем: а). В микросомах, с участием комплекса НАДН2-редуктаза-цитохром b5: 2НО-аскорбат-О· + НАДН2 → 2НО-аскорбат-ОН + НАД+ б). В митохондриях, с участием НАДН2-семидегидроаскорбатредуктазы: 2НО-аскорбат-О· + НАДН2 → 2НО-аскорбат-ОН + НАД+ в). В цитозоле, с участием НАДФН2-дегидроаскорбатредуктазы: О=аскорбат=О + 2НАДФН2 → НО-аскорбат-ОН + 2НАДФ+ г). В цитозоле, с участием GSH-дегидроаскорбатредуктазы: О=аскорбат=О + 2GSH → НО-аскорбат-ОН + GS-SG 2). взаимодействует с активными формами кислорода — О ∙ 2, Н2О2, НО ∙ и инактивирует их. β-Каротин, предшественник витамина А, также обладает антиоксидантным действием и ин-гибирует ПОЛ. Соединения, связывающие железо. Большинство из них, включая такие природные соединения как дипептид карнозин, не просто связывают железо, но, самое главное, не дают ему возможности приникнуть в липидную фазу мембран, поскольку образующиеся комплексы, в силу своей полярности, не проникают в гидрофобную зону. Для детоксикации двухвалентного железа в организме существует, по-видимому, целая система окисления и связывания ионов железа. В плазме крови эта система представлена ферментом церрулоплазмином (феррооксидазой), который окисляет Fe2+ до Fe3+ кислородом без образования свободных радикалов, и белком трансферрином, который связывает и переносит в кровяном русле ионы трехвалентного железа, которые затем захватывается клетками. В клетках железо может восстанавливаться аскорбиновой кислотой и другими восстановителями, но затем окисляется и депонируется в окисленной форме внутри ферментного белкового комплекса ферритина. Литература:
|