Энергия Гиббса и состояние химического равновесия
Рассмотрим как меняется энергия Гиббса веществ при равновесии химической реакции: аА(г) При достижении равновесия энергия Гиббса реакции станет равной нулю: ∆G реакции = b G B – а G А = 0илиа G А = b G B. (3.20)
При равенстве энергий Гиббса продуктов реакции и исходных веществ движущая сила реакции исчерпана, и реакция останавливается, т.е. парциальные давления (концентрации) всех веществ становятся постоянными и не меняются как угодно долго (при данных условиях). Такое состояние химической системы называется состоянием химического равновесия. Установившиеся при этом парциальные давления (концентрации) веществ называются равновесными. Запишем условие равновесия с учетом уравнений (3.16) и (3.20): a(G oА+ RT ln р A)=b(G oB+ RT ln р B). Для рассмотренной реакции: ∆G реакции=b(G oB+ RT ln p B)−a(G oА+ RT ln p A)=0,
Соотношение равновесных парциальных давлений − величина для данных условий постоянная и называется константой равновесия (Кр):
Следовательно, можно записать, что: ∆ G o p=−RTlnKp. (3.21) Константа равновесия равна отношению произведения равновесных парциальных давлений продуктов реакции и исходных веществ, возведенных в степени, равные стехиометрическим коэффициентам веществ в рассматриваемой реакции. Например, для реакции N2(г) + 3H2(г) 2NH3(г) константа равновесия запишется как
где р – равновесные относительные парциальные давления соответствующих веществ. Константу равновесия можно рассчитать, объединяя уравнения (3.17) и (3.21):
Из уравнения (3.24) видно, что Кр для данной системы зависит только от температуры. При данной температуре это величина постоянная и не зависит от первоначальных количеств взятых для реакции веществ. При использовании молярных концентраций веществ, участвующих в реакции, равновесие характеризуется концентрационной константой равновесия (Кс), которая равна отношению произведений равновесных концентраций продуктов реакции и исходных веществ, возведенных в степени, равные стехиометрическим коэффициентам веществ в рассматриваемой реакции. Например, для рассмотренной выше реакции константа равновесия запишется как
где, [N2], [NH3], [H2] - равновесные концентрации веществ, участвующих в реакции, моль/л. Если все реагенты газообразны и их поведение подчиняется закону идеальных газов, то связь между Кр и Кс можно выразить уравнением
где R − газовая постоянная, равная 0,082 л×атм/моль×К; Dn− изменение числа молей газообразных веществ в результате реакции: Dn=(b–а) − для приведенной выше реакции. Например, для реакции синтеза аммиака N2(г)+3H2(г) 2NH3(г) Dn=2–(1+3)=–2 и Кр = Кс (RT)-2. Если реакция идет без изменения объема (количества молей газообразных веществ в результате реакции не меняется) или реакция протекает в растворе, то Кр = Кс. Например, для реакции N2(г) + O2(г) 2NO(г), Кр = Кс. Парциальные давления (концентрации) твердых веществ, принимающих участие в реакции, в выражение константы равновесия не включаются. Например, для реакции MgCO3(тв) константа равновесия запишется как Кр = р
|

 bВ(г).
bВ(г).
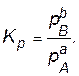

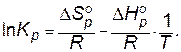 . (3.22)
. (3.22) ,
, , (3.23)
, (3.23) MgO(тв) + CO2(г)
MgO(тв) + CO2(г) , Kс =[CO2]равн.
, Kс =[CO2]равн. 



