Молекулярность и порядок реакции
Молекулярность реакции есть число частиц (атомов, молекул, ионов, радикалов), участвующих в элементарном акте. Например, реакция перегруппировки трифенил(триметилперокси)силана является мономолекулярной реакцией:
При горении водорода реакции зарождения, продолжения и разветвления цепи соответствуют бимолекулярным реакциям. В каждом элементарном акте участвуют две частицы, например Н× + О2 ® продукты реакции. Реакция обрыва цепи – тримолекулярная реакция. В каждом элементарном акте такой простой реакции участвуют три частицы (НО×, × Н и М): НО× + × Н + М ® Н2О + М* Роль третьей частицы М выполняет атом или молекула в стенке реактора или молекула в объеме реактора. Функция частицы М сводится к дезактивации образующейся молекулы Н2О. В результате тройного столкновения уменьшается кинетическая энергия, энергия колебательного движения атомов, способная разорвать связь в образовавшейся молекуле воды НО–Н. Часть колебательной энергии принимает на себя молекула М. Она переходит в возбужденное состояние М*, обеспечивая устойчивость молекулы воды. В соответствии с законом действия масс уравнения скорости элементарных химических реакций записываются следующим образом: для мономолекулярной реакции А ® продукты u = kcA для бимолекулярной реакции 2 А ® продукты А + В ® продукты u = kcAсВ для тримолекулярной реакции 2 А + В ® продукты B + 2 D ® продукты В общем виде для элементарной химической реакции nАА + nВВ ® продукты где ni – стехиометрические коэффициенты уравнения химической реакции, а ni – показатели степени, с которыми концентрации реагентов входят в уравнение закона действия масс. Для элементарных химических реакций стехиометрические коэффициенты и показатели степени, с которыми концентрации реагентов входят в уравнение скорости реакции, совпадают, т.е. nА = nA и nВ = nB. Показатель степени ni, с которым концентрация реагента входит в уравнение скорости реакции, обозначает порядок реакции по данному реагенту. Общий порядок реакции равен сумме показателей степеней концентраций всех реагентов, которые входят в кинетическое уравнение скорости реакции. Например, для бимолекулярной простой реакции общий порядок равен двум: nA + nB. = 1 + 1 = 2. Для мономолекулярной реакции превращения А в продукт реакции В: А ® В должно выполняться условие соударений как источник активационной энергии. Общепринятой схемой активирования молекул А в результате бимолекулярных соударений является схема Линдемана (1922 г.): А + А ® А* + А (k 1) бимолекулярная активация А* + А ® А + А (k 2) бимолекулярная дезактивация А* ® В (k 3) распад с образованием продукта Бимолекулярные процессы активации и дезактивации обеспечивают некоторую стационарную концентрацию активированных молекул А*. Энергия столкновения превращается в колебательную энергию активированной молекулы А*. Через некоторое время молекула А* либо дезактивируется, либо распадется с образованием продукта реакции В. Скорость расходования и образования активированных молекул в соответствии с принципом стационарности выражается уравнением:
или Скорость превращения А в В определяется скоростью реакции А* ® В:
Подставляя в это уравнение концентрацию сА* из уравнения (5.9), получим выражение для скорости мономолекулярной реакции:
При большой концентрации вещества А, когда скорость дезактивации во много раз больше скорости распада, т.е. * k 2 cAcA* > > k 3c A* или k 2 cAcA* > > k 3c A, первым слагаемым в знаменателе уравнения (5.10) можно пренебречь по сравнению со вторым. В результате получим:
или u = kcA, где Мономолекулярное превращение вещества подчиняется уравнению реакции первого порядка. Тримолекулярные элементарные реакции встречаются чрезвычайно редко. Вероятность тройного столкновения мала по сравнению со столкновениями двух частиц. Не имеет смысла говорить о молекулярности сложной реакции. Она включает главным образом элементарные моно- и бимолекулярные реакции. Для сложных реакций частный и общий порядок реакции выражается как целыми, так и дробными числами, которые находят экспериментально. Например, скорость сложной реакции H2(г)+ Br2(г) = 2HBr(г) описывается уравнением:
включающим целочисленные и дробные частные порядки. Сложная реакция H2(г)+ I2(г) = 2HI(г) является реакцией второго порядка
Формально наблюдается совпадение стехиометрических коэффициентов и частных порядков в уравнении скорости реакции. Но это лишь совпадение. Исследование механизма этой реакции показало, что образование HI включает моно- и тримолекулярные элементарные реакции.
|


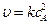
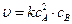

 ,
, (5.8)
(5.8) . (5.9)
. (5.9)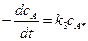 .
. . (5.10)
. (5.10) (5.11)
(5.11) .
.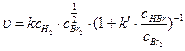 ,
,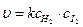 .
.


