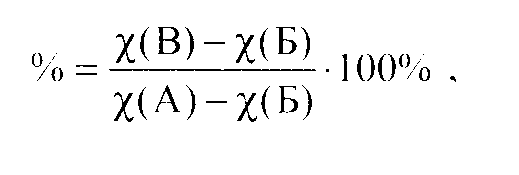Таратылатын материал. Көміртек {II) оксидін қанда анықтау жолы спектроскопиялық әдіс (Крамаренко В.Ф
Кө міртек {II) оксидін қ анда анық тау жолы спектроскопиялық ә діс ( Крамаренко В.Ф. Токсикологическая химия.- Выша школа.-Киев.-1989.-С.415-424) СО (II) мен уланғ андардың қ анындағ ы гемоглобин барлық мө лшерде карбоксигемоглобинге айналмайды. Уланудан ө лім оксигемоглобиннің карбоксигемоглобинге тү гел ауысудан анағ ұ рлым ерте тү седі.. Қ андағ ы карбоксигемоглобинді спектроскоппен анық тауғ а болады, бұ л-бірқ атар, соның ішінде карбоксигемоглобинді, заттарды спектральды визуальді анық тауғ а арналғ ан прибор. Қ анды спектроскоппен қ арағ анда карбоксигемоглобинның бар-жоқ тығ ын анық тауғ а мү мкіндік беретін сызық тар мен жолдар кө рінеді.. Зерттеуге арналғ ан қ анды сумен ашық -қ ызыл боялғ ан ерітінді алғ анша сұ йылтады. Бұ л ерітіндіні спектроскопиялы зерттелетін кезде сә йкес спектралды жолдар кө рінеді. Қ андағ ы оксигемоглобин ОНЬ спектрі 577-589 жә не 536-556 нм толқ ын ұ зындығ ындағ ы Фраунгофер D жә не Е сызық тары арасында 2 жұ тылу аймағ ына ие болады. Карбоксигемоглобиннің СОНЬ жұ тылу аймағ ы 564—579 жә не 523—536 нм толқ ын ұ зындығ ына сә йкес. Зерттелетін қ анның 4 кө леміне 1 кө лем (NH4)2S немесе басқ а тотық сыздандырғ ыштарды (дитионит натрия Na2S2O4 ) қ осқ ан кезде оксигемоглобин (ОНЬ) дезоксигемоглобинге НЬ ауысып, спектрінде жұ тылу аймағ ы 543—596 нм-ге сә йкес болады.Сондық тан да тотық сыздандырғ ыштарды қ осқ ан соң карбоксигемоглобиннің жұ тылу аймақ тары жоғ алып кетпейді. Окси жә не карбоксигемоглобин бар қ анғ а аммони сульфид ерітіндісін қ осқ анда НЬСО-ның 2 жұ тылу жолы қ олып, ОНЬ-ң жұ тылу жолдары жойылады. Қ андағ ы сә йкес жұ тылу жолдары бойынша СО (ІІ)-мен улану туралы қ орытынды жасайды. Спектральды анализ зерттелетін қ анда 10—30 % карбоксигемоглобин болса жү зеге асырылады. Оптикалық ә діс ( Калетина Н.И.-Метаболизм и определение токсиканто.-М.-ГЭОТАР-Медиа.-2008.-С. 753-759) СО-ғ а объектіні зерттеуге негізінен уланғ ан қ ан мен СО бар ө ндіріс ауасы алынады. Қ андағ ы НЬСО-ны зерттеудің ү лкен диагностикалық мә нге улану алдында алынғ ан қ ан ие болады, себебі науқ асқ а алғ ашқ ы дә рі-дә рмектермен кө мек кө рсеткен кезде СО мө лшері тө мендеп, қ андағ ы НЬСО мө лшері взаяды. СО-ны спектрофотометриялы анық тау кең таралғ ан себебі гемоглобинды қ ұ рылымдар аймағ ында абсорбцияғ а ие. Роке ә дісі тө мен концентрациялы НЬСО-ны анық таудағ ы қ олайлы ә діс болып табылады. Ол НЬ жә не НЬСОтотық сызданғ ан натрий гидросульфит спектрінің жұ тылу қ абілетін салыстыруғ а негізделген.НЬ жә не НЬСО гидросульфит натриймен байланыспайды. Спетрлерді қ анды (0, 1мл) аммиак ерітіндісімен (50мл) сұ йылтқ аннан кейін тү сіреді. НЬ жә не НЬСО абсорбциясын 420 жә не 432 нм-де ө лшейді.Алдын-ала 420 жә не 432нм-дей экстинкцияның молялы коэффициенті анық талынып алынады. 420 нм-де НЬСО абсорбциясы НЬ-ге қ арағ анда 2 есе жоғ ары, ал 432нм-де НЬ абсорбциясы НЬСО-ге қ арағ анда 3 есе жоғ ары. Арнайы формула арқ ылы қ ан қ ұ рамындағ ы НЬСО-ны анық тағ анда 420 жә не 432нм-дегі НЬ жә не НЬСО абсорбция айырмашылығ ы есептелінеді.Рооке ә дісін ө ткізу жә не математикалық есептеулері қ иын болғ анымен алынғ ан нә тижелері дә лірек анық талады. Спектроскопиялық ә діс. Спектроскопиялық (микроспектральді) анализ гемоглобин жә не оның туындыларының белгілі бір толқ ын ұ зындығ ында жарық жұ ту қ асиетіне негізделген. Қ ұ рамында гемоглобин жә не оның туындылары бар сұ йық тық тан жарық сә улесін ө ткізгенде спектрде қ ара жолақ тар пайда болады. Гемоглобиннің ә р туындысына тә н спектрдің арнайы бө ліктерінде жолақ тар шығ ады. Сот-медициналық тә жірибеде спектроскоп сияқ ты окулярмен қ осылғ ан микроспектроскоптарды қ олданады. Спектрде оксигемоглобиннің (НЬО) 2 жолағ ы λ 589— 577 жә не λ 556—536 нм-де, қ алпына келген гемоглобиннің (НЬ) λ 596—543 нм-де бір жолағ ы, ал НЬСО –ның λ 579—564 жә не λ 536—523 нм-де 2 жолағ ы бар.. Зерттеуге қ анды сумен сұ йылтады. Сұ йылтуды спектроскопта Фраунгофердің О жә не Е жазық тарының арасындағ ы жасыл жә не сары аймақ та 2 жолақ пайда болғ анша жалғ астырады. Бұ л жолақ тар НЬО сә йкес.Сұ йық тық қ а жаң а дайындалғ ан (Гм'Н4) қ осқ анда, НЬО редуцирленген гемоглобинге қ айта тотығ ады. Біраз уақ ыттан соң алдында пайда болғ ан 2 жолақ тың орнына, екеуінің ортасынан 1 кең жолақ пайда болады. Қ ұ рамында СО бар қ анды спетроскопиялық зерттегенде де, НЬСО-ғ а тә н 2 жолақ кө рінеді.. НЬСО жә не НЬО спектрлерін салыстырғ анда олардың жолақ тары сә йкес келмейді. НЬСО-ғ а аммоний сульфидің қ осқ анда, қ айта тотық пайды жә не пайда болғ ан 2 жолағ ы жоғ алып кетпейді. Уланғ ан кезде қ ан СО толық қ анық пайақ адам ө ліа кетеді.Сондық тан мә йіттің қ ан қ ұ рамында НЬСО мен қ атар НЬО-да кездеседі. Аммоний сульфидін қ осқ анда спектроскоптағ ы НЬСО-ның 2 жолақ тарының арасында кү ң гірттену- қ алпына келген гемоглобин жолағ ы пайда болады. Колориметрлік ә діспен қ ан қ ұ рамындағ ы НЬСО сандық анық тау. (модифицирленген Вольф ә дісі). Бұ л ә діс НЬО-ның НЬСО-ғ а қ арағ анда 15 минут ішінде рН 4, 95. температура 55—60 " С болғ анда тұ нбағ а тү суіне негізделген. Ал НЬСО-ның тұ нбасына кө бірек уақ ыт керек. Сө йтіп, осы 2 затты бө ліп алып НЬСО-ны колориметриялық анық тайды. Қ ұ рамында гемоглобині анық талғ ан қ анды ә ртү рлі дә режеде сұ йылта отырып, колибрлі қ исық қ ұ рады..Зерттелетін қ анды 50— 100 есе сұ йылтып, жарық ты жұ тылуына жә не калибрлі қ исық қ а қ арай отарып, гемоглобин концентрациясы анық талады. Гемоглобиннің СО-мен қ анығ у пайызын тиісті формуламен анық талады. СО-ны Вольфә дісімен анық тауды уланудан пайда болғ ан ө лімнен кейін тез арада ө ткізу қ ажет. Себебі, ұ зақ уақ ыттан кейін молекулалардың белокты бө лігі ө згеріп, гемопротеиндермен НЬСО-ның ерігіштігі ө згереді.. Фревурст — Майнекенің спектрофотометриялық ә дісі. Бұ л ә діс гемолизденген қ анның белгілі толқ ын ұ зындық тарында (X 575 немесе 578 нм). Жарық жұ ту қ абілетіне негізделген. Ол НЬО гидросульфат натриймен тотық сызданғ анғ а дейін жә не кейін ө ткізіледі. Қ анның 100% СО-ғ а қ анық қ ан кездегі жарық жұ ту қ абілеті натрий гидросульфитін қ осқ аннан кейінде ө згермейді. Егер қ анның қ ұ рамы СО-ғ а толық қ анық паса немесе СО болмаса, ол азаяда. Оның азаю дә режесіне байланысты НЬСО-ның пайызын анық тайды. Клинико-химиялық зертханалар автоматтандаралғ ан дифференциалды спектрофотометрлермен жабдық талғ ан. Олар біруақ ытта гемолизденген қ анның 4 жә не одан да кө п толқ ын ұ зындық тарында жалпы гемоглобин мө лшерін, НЬО жә не НЬСО пайыздық қ атынасын жә не метгемоглобинмен сульфагемоглобиннің оптикалық тығ ыздығ ын ө лшейді. Спектрофотометриялық ә діспенқ андағ ы карбоксигемоглобинді анық тау. Зерттелетін қ анғ а тотық тырғ ыш (натрий тиосульфат) қ осқ аннан кейін окси- жә не мет-гемоглобиннен тотық қ ан гемоглобин тү зіледі.Соң ғ ысының жұ ту спектрі 8-16, Б суретінде кө рсетілген.. Оттегіге қ арағ анда СО газы гемоглобинге ұ қ сас болғ андық тан, НЬСО-кешені натрий тиосульфатқ а бұ зылмайды. Сондық тан НЬСО кешенін натрий тиосульфатпен ө ң дегенде ө зіне тә н 2 жұ тылу жолағ ы кө рінеді. (сурет. 8-16, А). А жә не Б спектрлерінің оптикалық тығ ыздығ ының максимальді ерекшелігі 540 нм толқ ын ұ зындығ ында байқ алса, ал 579 нм толқ ын ұ зындық тарында олар шамалас тең келеді. Қ ан қ ұ рамындағ ы СО-ның пайыздық мө лшері (8-16. А сурет) анық тауғ а болады: қ ұ рамында НЬСО жоқ, сау оптикалық тығ ыздық мө лшерінің (8-16. Б суреті) мә ні жә не натрий тиосульфаты қ осылғ аннан кейінгі зерттелетін ү лгі (8-16. В сурет) қ атынасымен:
где х — оптикалық тығ ыздығ ы.. 8-16 сурет. А-НЬСО уф спектрлері, Б-қ алпына келген гемоглобина, В-кө міртегі оксидімен уланғ ан паписта қ аны.
Нә тижелердің интерпретациясы • Қ андағ ы СО дең гейі < 5%: қ алыпты; темекі тартатындар 10% дейін. • Қ андағ ы СО дең гейі 10—20%: жең іл дә режедегі интоксикация. • Қ андағ ы СО дең гейі 20—30%: орташа дә режелі интоксикация. • Қ андағ ы СО дең гейі 30—40%: орташа дә режелі интоксикация, бірақ коллапс болуы мү мкін. • Қ андағ ы СО дең гейі 40—50%: орташа дә режелі интоксикация, тыныс алу жә не жү рек-қ ан тамырлар жү йесі зақ ымдалады, жиі колапс болады, қ айтыс болуы мү мкін. • Қ андағ ы СО дең гейі 50—60%: ауыр дә режелі интоксикация — кома, талмалар, қ айтыс болуы мү мкін.. • Қ андағ ы СО дең гейі 60—90%: қ айтыс болады.
Ә дебиеттер: 1. Токсикологическая химия: метаболизм и анализ токсикантов: учебное пособие + СD/ под ред. Н.И. Калетиной. – М., 2008. – 1016 с. Переплет. 2. Токсикологическая химия: учебник / под ред. Т.В. Плетеневой. – 2-ое изд. – М., 2008. – 512 с. Переплет. 3. Лужников Е.А. Клиническая токсикология. -М., " Медицина", 1994. –189с.
Бақ ылау сұ рақ тары: 1. Қ анда кө міртек (II) оксидін анық таудың оптикалық ә дістері. 2. Қ анда кө міртек (ІІ) оксидін анық таудың спектроскопиялық ә дісі. 3. Қ анда НbСО аз концентрациясын анық тау Рооке ә дісі. 4. Қ анда НbСО колориметриялық ә діспен сандық анық тау 5. Фревурста — Майнектің спектрофотометриялық ә дісі. Тақ ырып 4 – Кө міртек оксидін талдауда газдысұ йық тық ә дісін қ олдану. Сандық мө лшерін анық тау қ орытындыларын бағ алау. Талдау қ ұ жаттары. Оқ у мақ саты: Карбоксигемоглобиннің химиялық анализ ә дістері жайлы білімді студенттерде қ алыптастыру. Ө ткізу тү рі: топтық презентация ө ткізу, сабақ нә тижелерін талдау. Тақ ырып бойынша тапсырмалар: кө міртек оксидінің талдау жолы газдысұ йық хроматография ә дістің презентациясы
|