Химические свойства. Для алкинов характерны реакции присоединения, замещения, окисления и полимеризации
Для алкинов характерны реакции присоединения, замещения, окисления и полимеризации. 1. Реакции присоединения: а) Гидрирование. Алкины, присоединяя водород в присутствии катализатора (Pt или Ni), переходят в алканы, а с катализаторами Pd или Fe – в алкены: НС≡ СН + 2Н2 б) Галогенирование. Реакции протекают ступенчато, с последовательным разрывом кратных связей: НС≡ СН + Br2 → CHBr=CHBr CHBr=CHBr + Br2 → CHBr2− CHBr2 1, 2-дибромэтен 1, 2-тетрабромэтан Обесцвечивание бромной воды, как и в случае алкенов, является качественной реакцией на кратную связь. в) Гидрогалогенирование. Процесс протекает легко и в две стадии: НС≡ СН + HCl → Н2С=СНCl Н2С=СНCl + HCl → H3C− CHCl2 хлорэтен (винилхлорид) 1, 1-дихлорэтан
виниловый спирт уксусный альдегид
бутин-1 бутен-1-ол-2 бутанон 2. Реакции замещения. Водород, связанный с атомом углерода при тройной связи, способен замещаться на металл с образованием ацетиленида: НС≡ СН + 2[Ag(NH3)2]OH → AgC≡ CAg + 4NH3 + 2H2O ацетиленид серебра НС≡ СН + 2[Cu(NH3)2]OH → CuC≡ CCu + 4NH3 + 2H2O ацетиленид меди Образование ацетиленидов – качественная реакция на тройную связь. 3. Реакции окисления. Алкины легко окисляются. Например, они обесцвечивают раствор перманганата калия: 3НС≡ СН + 8KMnO4 + 4H2O → 3НООC− СООН + 8KOH + 8MnO2↓ щавелевая кислота Эта реакция используется как качественная на тройную связь.
|

 Н3С− СН3 НС≡ СН + Н2
Н3С− СН3 НС≡ СН + Н2 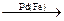 Н2С=СН2
Н2С=СН2 г) Гидратация (реакция Кучерова). В этой реакции в качестве катализатора используют соли ртути HgSO4 или Hg(NO3)2:
г) Гидратация (реакция Кучерова). В этой реакции в качестве катализатора используют соли ртути HgSO4 или Hg(NO3)2: НС≡ СН + Н2О
НС≡ СН + Н2О  →
→ Гомологи ацетилена гидратируются легче, чем ацетилен. Реакция идет по правилу Марковникова с образованием кетонов:
Гомологи ацетилена гидратируются легче, чем ацетилен. Реакция идет по правилу Марковникова с образованием кетонов: Н3С− СН2− С≡ СН + Н2О
Н3С− СН2− С≡ СН + Н2О 


