Молекуланың еркін жүру жолының орташа ұзындығы
Жылулық қозғалыстағы газ молекулалары бір-бірімен үздіксіз соқтығысады. Соқтығысқанша олар l жолды еркін жүреді. Еркін жүру жолы – кездейсоқ шама. Тетелес екі соқтығысудың арасындағы осы жол ұзындығы әр түрлі болады, бірақ молекулалардың саны өте көп және олардық қозғалысында ешқандай тәртіп болмайтындықтан, молекулалардың еркін жолының орташа ұзындығы деген ұғым ендіреміз, оны Енді
Соқтығысулардың орташа саны:
Мұндағы d – соқтығысу кезінде екі молекула центрлерінің арсындағы ең аз қашықтықтағы молекуланың эффективті диаметрі деп аталады. Молекулалардың жылдамдықтары температура жоғарылағанда артып, эффективті диаметр шамамен молекуланың эффективті қимасы σ – ға тең болады:
Енді молекуланың еркін жүру жолының орташа мәнін келесі формула арқылы анықтайық:
Немесе эффективті диаметрді (d) молекуланың эффектвті қимасымен алмастырсақ:
Сонымен еркін жүру жолының орташа мәні газдың абсолют температурасына тәуелді емес, себебі Т артқан сайын, газ молекулаларының орташа жылдамдықтарымен (
|

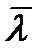 деп белгілейік. Енді осы орташа еркін жүру жолының ұзындығын есептеп шығарайық.
деп белгілейік. Енді осы орташа еркін жүру жолының ұзындығын есептеп шығарайық. болсын дейік. Егер 1 секунд ішінде ол
болсын дейік. Егер 1 секунд ішінде ол  рет соқтығысатын болса, онда орташа епкін жүру жолының шамасы:
рет соқтығысатын болса, онда орташа епкін жүру жолының шамасы: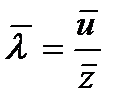 .
.

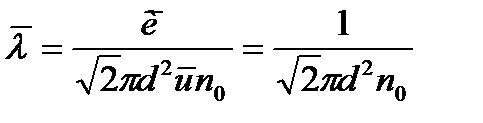
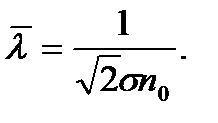
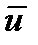 ) қатар оның соқтығысу саны
) қатар оның соқтығысу саны  - ге артып отырады.
- ге артып отырады.


