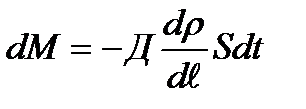Тасымалдау құбылысы
Белгілі көлемдегі газ молекулалары бір орыннан екінші орынға диффузия арқылы ауысады, энергия жылу өткізгіштік және импульс ішкі үйкеліс нәтижесінде беріледі. Жоғарғы айтылған үш құбылыстың үшеуінде де біз белгілі бір шаманы: молекула массасын, оның энергиясын және қозғалыс мөлшерін тасымалдаймыз. Сондықтан да бұл құбылыстар – тасымалдау құбылыстары деп аталады. Енді осы айтылған тасымалдау құбылыстарының заңдылықтарын жеке қарстырайық. 1. Диффузия құбылысы. Айталық, берілген газ тығыздығы ρ көлемнің әр жерінде түрліше болсын. Мысалы, суретте көрсетілген дөңес 1 – беттің кез келген нүктесінің тығыздықтары бірдей ρ – ға тең де, осы сияқты 2 – беттің тығыздығы ρ + ∆ ρ болсын.
Сурет
Енді 1 – беттің кез келген нүктесінен тығыздықтың өсу бағытына қарай нормаль n кесіндісін тұрғызайық. Тығыздықтары бірдей екі беттің ара қашықтығын нормаль бағыты бойынша
Енді нормаль n – ге перпендикуляр болатындай S ауданшасын белгілейік. S ауданшасының екі жағындағы газ молекулаларының тығыздығы әр түрлі, себебі ауданшадан солдан оңға қарай немесе оңнан солға қарай бағыттлып өтіп жатқан молекулалар сандары бірдей емес. Сондықтан осындай молекулалар санын, яғни Диффузия құбылысы деп, тиісіп тұрған екі заттың (газ, сұйық немесе қатты денелер) атомдары немесе молекулаларының бір-біріне өтуін айтады. Швейцар физигі Фик (1885 ж) тағайындаған заң бойынша, бірлік уақыт аралағында S ауданшадан өтетін заттың массасы
Мұндағы минус таңбасы диффузияның газ тығыздығының кему жағына бағытталуын көрсетеді. D – диффузия коэффициенті, газ күйінің тегіне байланысты. Ол 1 Газдардың кинетикалық теориясына байланысты
Мұндағы v – молекуланың орташа арифметикалық жылдамдығы, 2.Жылу өткізгіштік құбылыс. Макроскопиялық тұрғыдан қарағанда жылу өткізгіштік құбылысы Q жылу мөлшерінің жылырақ қабаттан суығырақ қабатқа ауысуы болып табылады. Суретте көрсетілген S ауданшаның екі жағының температурасы әр түрлі, яғни І беттің температурасы Т да, ІІ беттің температурасы Т+∆Т болсын. Сонда температура градиенті
Бұл шама изотермиялық беттегі нормаль бойынша өзгеретін газ температурасының градиенті болып табылады, яғни жылдамдығы артқан газ молекулаларының орташа кинетикалық энергиясы көп болса, оның температурасы жоғары болады. Олай болса, S ауданшасы арқылы dt уақыт ішінде өтетін жылу мөлшері
минус таңбасы жылу мөлшерінің азаюын көрсетеді.
Сурет Мұндағы
Мұндағы
(3) формула газ молекулаларының жылу түрінде тасымалданатын энергиясын сипаттайды да, француз физигі Фурьенің (1768 - 1880) жылу өткізгіштік заңы деп аталады. 3. Газдардың ішкі үйкелісі (тұтқырлығы). Газдардың немесе сұйықтардың ламинарлық ағысын қарастырғанда, әр түрлі қабаттардың жылдамдықтары түрліше болады дедік. Олай болса, қатар жатқан екі қабаттың арасындағы шекарада ішкі үйкеліс күші пайда болады. Осы күштің шамасы Ньютон тағайындаған заңдылық бойынша анықталады:
Мұндағы минус таңбасы үйкеліс күшінің қабаттар жылдамдығына қарама-қарсы екенін көрсетеді, η – тұтқырлық немесе ішкі үйкеліс коэффициенті, ол (Па с) – пен өлшенеді. Ал dU/dc – жылдамдық градиенті, S – күш түсірілген беттің шамасы. Газдардың кинетикалық теориясына сүйене отырып, ішкі үйкеліс коэффициентін анықтаймыз:
Мұндағы ρ – газ тығыздығы, Идеал газдар үшін диффузиялық, жылу өткізгіштік және ішкіүйкеліс коэффициенттері өзара байланыста болады: η = ρД,
Сонымен Д, 1 – кесте
|





 деп белгілейік. Сонда
деп белгілейік. Сонда  қашықтықтағы газ тығыздығының өзгерісі
қашықтықтағы газ тығыздығының өзгерісі  екндігін ескерсек, онда
екндігін ескерсек, онда  /
/ 
 бір моолекуланың масасына
бір моолекуланың масасына 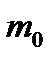 көбейтсек, тығыздықтың кему бағытына тасымалданған газ массасын білеміз.
көбейтсек, тығыздықтың кему бағытына тасымалданған газ массасын білеміз. (5.15)
(5.15) - пен өлшенеді.
- пен өлшенеді. (5.16)
(5.16) - орташа еркін жүру жолы.
- орташа еркін жүру жолы.
 (5.17)
(5.17)
 - газдың тегіне тәуелді, жылу өткізгіштік коэффициенті деп аталады. Жылу өткізгіштік коэффициенті Вт/(мК) – мен өлшенеді. Газдардың молекула – кинетикалық теориясына байланысты бұл коэффициент:
- газдың тегіне тәуелді, жылу өткізгіштік коэффициенті деп аталады. Жылу өткізгіштік коэффициенті Вт/(мК) – мен өлшенеді. Газдардың молекула – кинетикалық теориясына байланысты бұл коэффициент: , (5.18)
, (5.18) - молекуланың орташа еркін жүру жолы,
- молекуланың орташа еркін жүру жолы,  - орташа жылдамдық,
- орташа жылдамдық, - газ молекуклаларының тығыздығы,
- газ молекуклаларының тығыздығы,  - тұрақты көлемдегі меншікті жылу сыйымдылық.
- тұрақты көлемдегі меншікті жылу сыйымдылық. (5.19)
(5.19) . (5.20)
. (5.20) - молекулалардың орташа жылдамдығы,
- молекулалардың орташа жылдамдығы,  - молекулалардың орташа еркін жүру жолының ұзындығы.
- молекулалардың орташа еркін жүру жолының ұзындығы.
 коэффициенттерінің өрнектеріне молекуланың
коэффициенттерінің өрнектеріне молекуланың  ұзындығының мәні еніп отырады (1 - кесте). Олай болса, осы үш коэффициенттің кез келген біреуінің сан мәні бойынша молекулалардың
ұзындығының мәні еніп отырады (1 - кесте). Олай болса, осы үш коэффициенттің кез келген біреуінің сан мәні бойынша молекулалардың