Вычисление Dt
Типичный вид температурной кривой правильно поставленного калориметрического опыта при измерении экзотермического эффекта показан на рис.1. Величину Dt с учетом теплообмена можно рассчитать аналитическим или графическим способом. При графическом определении Dt на миллиметровой бумаге на оси абсцисс откладывается время в масштабе 1 мин-1см, на оси ординат - температуру, выбор масштаба которой зависит от величины Dt. При Dt£1o 1o =10cм; Dt³1o 1o =5cм. После того как на график нанесены все экспериментальные точки, получается кривая АBCD. Участок АВ называется начальным периодом, ВС - главным, СD - конечным. Чтобы определить изменение температуры Dt, не искаженное теплообменом, происходящим в течение главного периода, продолжают АВ и CD до пересечения с вертикальной прямой EF. Для этого точки m и n, соответствующие начальной и конечной температурам главного периода, наносят на ось ординат. Через середину отрезка mn проводят линию КР. Пересечение этой линии с кривой ВС дает точку l, определяющую положение прямой EF. Отрезок EF и будет равен Dt, отрезок mn -Dt¢. Чем меньше температурный ход в начальном и конечном периодах, тем меньше потери теплоты за счет теплообмена и тем ближе Dt к Dt¢. Характер линии ВС зависит от условий протекания теплового процесса (например, от размешивания), наклон линий АВ и ВС зависит от характера теплообмена с окружающей средой. Таким образом, по виду кривой АВСD можно судить о качестве проведенного опыта.
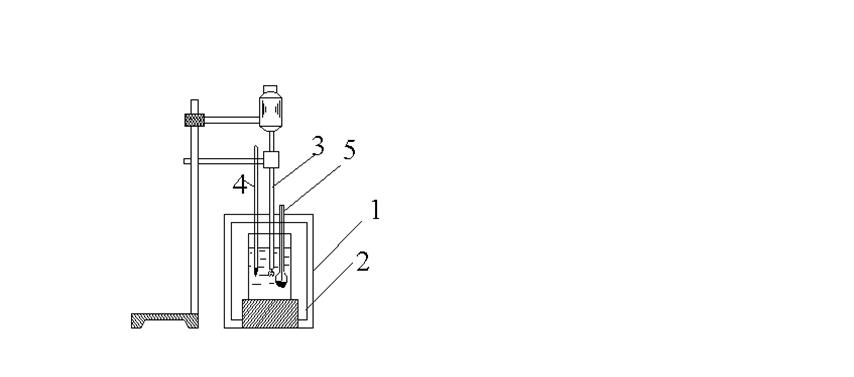
3.ОПРЕДЕЛЕНИЕ ИНТЕГРАЛЬНОЙ ТЕПЛОТЫ РАСТВОРЕНИЯ СОЛИ Тепловой эффект, сопровождающийся растворением твердого вещества в жидкости и отнесенный к 1 г растворяемого вещества, называют удельной теплотой растворения (q). Тепловой эффект, отнесенный к 1 моль растворяемого вещества, называют молярной теплотой растворения (Q). Теплота растворения зависит от концентрации раствора. Различают интегральную теплоту растворения - тепловой эффект, сопровождающий процесс растворения 1 моль (молярная) или 1 г (удельная) вещества в данном количестве растворителя; и дифференциальную теплоту растворения - тепловой эффект, сопровождающий процесс растворения 1 моль вещества в бесконечно большом количестве раствора заданной концентрации. Интегральные теплоты растворения определяют экспериментально, а дифференциальные вычисляют по зависимости интегральных теплот растворения от концентрации раствора. Определение величины теплового эффекта растворения соли выполняют в калориметре, простейшее устройство которого приведено на рис.2. Для определения теплового эффекта растворения соли в калориметрический стакан (2) наливают воду, в тонкостенную ампулу (5) помещают соль. После выравнивания их температур ампулу разбивают и измеряют изменение температуры калориметра, вызванного растворением соли в воде.
Рис.2. Устройство калориметра: 1- термоизолирующий стакан с крышкой; 2- стакан калориметра, установленный на термоизолирующую подставку; 3- мешалка; 4- термометр с ценой деления 0.1oС; 5- ампула с вводимым веществом и стеклянной палочкой. Интегральную удельную теплоту растворения определяют по формуле: q=Dt W, (7) где Dt - изменение температуры системы, вызванное прошедшим процессом, W - водяное число калориметра. По физическому смыслу W представляет собой количество граммов воды, теплоемкость которой равна теплоемкости калориметра, или количество тепла, требующееся для нагревания калориметра но 1оС. Простейшими методами определения водяного числа калориметра являются следующие: а) Расчетный метод - рассчитывают теплоемкость каждой части калориметра, перемножая ее вес (mi) на удельную теплоемкость материала, из которого она состоит (Сi): W=å mi Сi (8) б) Электрический метод- с помощью электронагревателя повышают на 1-1.5о температуру калориметрической системы. Определив при этом изменение температуры Dtэ и тепло, которое получила система в результате электронагрева qэ= 0.239 I E t, (9) рассчитывают водяное число калориметра по формуле: W= qэ/Dtэ = 0.239 I E t/Dtэо, (10) где I - сила тока, Е - падение напряжения на клеммах нагревателя, t - время пропускания тока, D tэо - истинное изменение температуры калориметра. в) Опытный метод - в калориметре осуществляется процесс, тепловой эффект которого q1 уже точно известен, определяют при этом изменение температуры Dt1 и рассчитывают водяное число калориметра по формуле: W= q1/Dt1. (11)
|