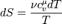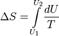Билет 13.
Поскольку в системе при изохорном процессе происходит теплообмен с внешней средой, то происходит изменение энтропии.
Изменение энтропии при квазистатическом изобарном процессе равно
В случае, если изобарный процесс происходит в идеальном газе, то dU = d(νCvT + νRT) = ν(Cv + R)dT = νCpdT, следовательно, изменение энтропии можно выразить как Если пренебречь зависимостью Cp от температуры, то Изотермический процесс
Термодинамическая вероятность— число способов, которыми может быть реализовано состояние физической системы. Уравнение Больцмана связывает энтропию S идеального газа и термодинамическую вероятность — величину W, которая равна количеству микросостояний, соответствующих данному макросостоянию системы(статистический вес)
Иначе говоря, формула Больцмана показывает отношение между энтропией и числом способов конструирования данной системы из атомов или молекул.
Правило, позволяющее определить, в каком именно направлении будет идти процесс при заданных условиях, называется вторым началом термодинамики. Разные состояния тела, соответствующие различному расположению молекул (атомов, ионов) и разным значениям их скоростей, осуществляются с очень разной вероятностью. По самому смыслу понятия вероятности любая система, предоставленная сама себе (то есть изолированная), будет переходить из состояния с меньшей вероятностью в состояние, вероятность которого больше. Обратный переход в принципе возможен, но практически невероятен. Учитывая формулу Больцмана, мы сразу приходим к формулировке второго начала термодинамики: все реальные процессы в изолированной системе происходят в сторону состояний с большей вероятностью, то есть с увеличением энтропии. Таким образом, второе начало является вероятностным законом.
|


 - молярная теплоемкостью при постоянном объеме.
- молярная теплоемкостью при постоянном объеме.