Билет 2,3,4,5,6.
1ое начало термодинамики Представляет собой закон сохранения энергии для систем, в которых существенное значение имеют тепловые процессы. Изменение внутренней энергии системы при переходе её из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе. Уравнение состояния идеального газа(уравнение Клапейрона — Менделеева)
формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа Работа и внутренняя энергия. Таким образом, одним из процессов, приводящих к изменению внутренней энергии, является преобразование механической энергии во внутреннюю или наоборот. Работа является мерой изменения внутренней энергии при превращении механической энергии во внутреннюю или внутренней энергии в механическую. точки зрения молекулярно-кинетической теории внутренняя энергия вещества складывается из кинетической энергии всех атомов и молекул и потенциальной энергии их взаимодействия друг с другом. В частности, внутренняя энергия идеального газа равна сумме кинетических энергий всех частиц газа, находящихся в непрерывном и беспорядочном тепловом движении.
А1 = р∆V – работа газа.
А1 = -А = р∆V – работа внешних сил. Теплоемкость Теплоёмкость тела (обычно обозначается латинской буквой C) — физическая величина, определяющая отношение бесконечно малого количества теплоты δQ, полученного телом, к соответствующему приращению его температуры δT:
Изотермический процесс/Изобарный/Изохорный/Адиабатный (см. в тетради)
Адиабатический процесс для идеального газа описывается уравнением Пуассона.
|




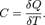
 Это уравнение Майера для одного моля газа.
Это уравнение Майера для одного моля газа.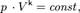
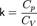 - показатель адиабаты.
- показатель адиабаты.




