Билет 8.
Внутреннюю энергию тела нельзя измерить напрямую. Можно определить только изменение внутренней энергии:
где
В теории идеального газа потенциальная энергия взаимодействия молекул считается равной нулю. Поэтому внутренняя энергия идеального газа определяется кинетической энергией движения всех его молекул. Средняя энергия движения одной молекулы равна
Так как в одном киломоле содержится
Учитывая, что Для любой массы m газа, т.е. для любого числа киломолей
Из этого выражения следует, что внутренняя энергия является однозначной функцией состояния и, следовательно, при совершении системой любого процесса, в результате которого система возвращается в исходное состояние, полное изменение внутренней энергии равно нулю. Равномерное распределение энергии по степеням свободы газовой молекулы: В классической статистической физике выводится закон Больцмана о равномерном распределении энергии по степеням свободы молекул: для статистической системы, находящейся в состоянии термодинамического равновесия, на каждую поступательную и вращательную степени свободы приходится в среднем кинетическая энергия, равная kT/2, а на каждую колебательную степень свободы — в среднем энергия, равная kT. Колебательная степень «обладает» вдвое большей энергией потому, что на нее приходится не только кинетическая энергия (как в случае поступательного и вращательного движений), но и потенциальная, причем средние значения кинетической и потенциальной энергий одинаковы. Таким образом, средняя энергия молекулы.
Так, мы получили Условия применимости распределения Максвелла: 1. Равновесное состояние системы, состоящей из большого числа частиц. 2. Изотропная система. 3. Классическая система. Это значит, что система должна быть не релятивистской и не квантовой (взаимодействие частиц допускается, но только зависящее от относительного положения частиц). Постоянная Больцмана - физическая постоянная, определяющая связь между температурой и энергией.
Универсальная газовая постоянная определяется как произведение постоянной Больцмана на число Авогадро, R = kNA. Газовая постоянная более удобна, когда число частиц задано в молях. Молярные теплоемкости идеального газа Молярная теплоемкость — теплоемкость 1 моля идеального газа.
|


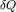 — подведённая к телу теплота, измеренная в джоулях
— подведённая к телу теплота, измеренная в джоулях — работа, совершаемая телом против внешних сил, измеренная в джоулях
— работа, совершаемая телом против внешних сил, измеренная в джоулях
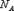 молекул, то внутренняя энергия одного киломоля газа будет
молекул, то внутренняя энергия одного киломоля газа будет
 , получим
, получим 
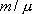 внутренняя энергия
внутренняя энергия
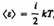
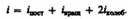

 - функцию плотности вероятности, которая и называется распределением Максвелла.
- функцию плотности вероятности, которая и называется распределением Максвелла. Дж/К
Дж/К




