Количественные характеристики адсорбции
Для количественного описания адсорбции применяют 3 величины. 1) Избыточная, или гиббсовская адсорбция Гi. Это избыток i-ого компонента в поверхностном слое по сравнению с его количеством в объеме фазы, приходящийся на ед. площади поверхности: Гi= Где Сis и Сi – молярная концентрация i-ого компонента в соответственном поверхностном слое и объеме фазы; Vs- объем поверхностного слоя, который принято считать двухмерным и равным 1 см2; S1,2- площадь поверхностного слоя. Учитывая, что молярная концентрация, умноженная на объем,- это количество вещества, Гi = 2) Абсолютная адсорбция. В тех случаях, когда способность вещества к адсорбции резко выражено, и в следствие этого Аi= Где 3) Удельная адсорбция. В тех случаях, когда измерить площадь поверхности αi = Если Гi, Ai, αi если Гi, Ai, αi Помимо этих количественных характеристик, адсорбцию газа можно характеризовать: 1) Зависимостью количества адсорбированного вещества А (Г) от температуры при постоянных Р или С А= f (Т), р=const, c=const. (изобары) 2) Зависимостью равновесного давления (или С) от температуры при постоянном количестве адсорбированного вещества: р= f (T), C= f(T), при A= cons. (изостеры) 3) Зависимостью количества адсорбированного вещества А от Р (или С) при постоянной температуре: А= f(Р), А=f(C), при T=const. (изотермы) Изотермы имеют особенно большое значение при изучении адсорбции.
|

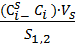 ,
,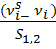 моль/дм2
моль/дм2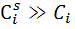 и
и 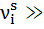
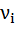 , адсорбцию характеризуют величиной Аi – абсолютная адсорбция:
, адсорбцию характеризуют величиной Аi – абсолютная адсорбция: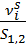 моль/дм2, всегда Аi
моль/дм2, всегда Аi 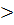 0,
0,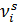 - количество вещества в поверхностном слое.
- количество вещества в поверхностном слое.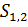 трудно, количество i-ого компонента
трудно, количество i-ого компонента 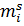 ) относят к массе адсорбента m используя величину удельной адсорбции αi:
) относят к массе адсорбента m используя величину удельной адсорбции αi: моль/г или αi =
моль/г или αi = 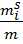 кг/ кг
кг/ кг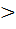 0,- положительная адсорбция,
0,- положительная адсорбция,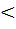 0,-отрицательная адсорбция.
0,-отрицательная адсорбция.


