Теоретическое введение. Все вещества, неорганические и органические, можно классифицировать, то есть выделить группы веществ
Технологический институт
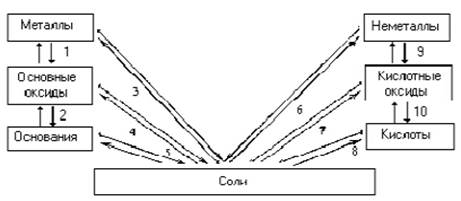
Все вещества, неорганические и органические, можно классифицировать, то есть выделить группы веществ, сходные либо по свойствам, либо по строению. Признак, по которому вещества делят на группы (классы), называется классификационным признаком. Так, основываясь на составе, можно разделить вещества на простые и сложные. Простые, в свою очередь, на металлы и неметаллы, а сложные – на оксиды, основания, кислоты, соли и др. Возможна также классификация соединений по другим классификационным признакам. Например, оксиды, на основании проявляемых ими кислотно-основных свойств, можно разделить на следующие классы: – основные оксиды CaO, MgO, Li2O; – амфотерные оксиды Al2O3, ZnO, Cr2O3, PbO; – кислотные оксиды СО2, SO3, Mn2O7, P2O5; – несолеобразующие (индифферентные) CO, NO, N2O,WO2, TiO2. На основании того же классификационного признака (кислотно-основных свойств) можно разделить и гидроксиды: – основания Ca(OH)2, Mg(OH)2, LiOH, Cu(OH)2; – амфотерные гидроксиды Al(OH)3, Zn(OH)2, Cr(OH)3; – кислоты H2SO4, H3PO4, HMnO4. Кроме того, те же оксиды можно классифицировать по их окислительно-восстановительным свойствам, агрегатному состоянию и т.д. На схеме (рис. 1) представлена связь между основными классами неорганических соединений. Данная схема позволяет предложить пути получения одних классов соединений из других и оценить возможность их взаимодействия друг с другом.
Рис. 1. Связь между основными классами неорганических соединений
|