Дезоксикортикостерон-ацетат
Desoxycorticosteronum aceticum. Desoxycorticosteroni acetas. Desoxycortoni acetas. Дезоксикортикостерон-ацетат. 11-дезоксикортикостерон-21-ацетат. С23Н32О4. М = 372,51.
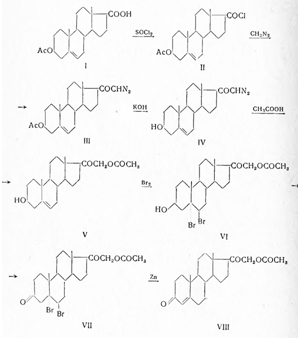
Синонимы: Соrtеnil, Соrtехоn, Соrtiron, DОСА и др. В отличие от многих кортикоидов, дезоксикортикостерон получен впервые в 1937 г. не изолированием из органов, а полусинтетическим путем (Штейгер, Рейхштейн) из 3β-ацетокси-5-этиеновой кислоты (I) — побочного продукта окисления 5,6-дибром-3-ацетата холестерина при синтезе дегидроэпиандростерона. С помощью тионилхлорида кислота эта превращена в хлорангидрид (II) и затем с помощью диазометана в диазокетон (III). При гидролизе 3-ацетильной группы едкой щелочью получен (IV), который ацетолизом превращен в 21-ацетокси-5-прегнен-3-ол-20-он. После присоединения одной молекулы брома образующийся дибромид (VI) окислен хромовой кислотой до 3-кетопроизводного (VII) и дебромированием цинковой пылью получен дезоксикортикостерон-ацетат (VIII):
В дальнейшем метод этот (1940) был улучшен; диазокетон по Оппенауэру окислен до 21-диазопрогестерона (IV) и затем уже ацетолизом превращен в дезоксикортикостерон-ацетат (VIII). Как показал далее Рейхштейн, 3-кето-4-этиеновая кислота (X), полученная окислением хромовой кислотой Зβ-окси-5-этиеновой кислоты (IX), после предварительного присоединения брома к двойной связи и последующего дебромирования, может быть превращена в 21-ацетоксипрегнан-3,20-дион (XIII), при бромировании с заменой водорода у С4 (XI) и отщеплении бромистого водорода с помощью пиридина (XII), а также других реакций, описанных ранее:
Вилдс и Шунк (1948) показали, что при действии оксалилхлорида на натриевую соль 3-кето-4-этиеновой кислоты (X) образуется хлорангидрид, который диазометаном переводят в 21-диазопрогестерон и действием затем уксусной кислоты в дезоксикортикостерон-ацетат. Лучшие выхода получены Шормом и Черни (1952) при присоединении цианистого водорода к дегидроэпиандростерон-ацетату, отщеплении воды и селективном гидрировании дегидронитрила в присутствии Рd-СаСO3. При гидролизе образуется кислота I:
Еще в 1939 г. дезоксикортикостерон-ацетат был получен из дегидроэпиандростерона присоединением ацетилена, с частичным гидрированием 17-виниландростен-3,17-диола и его окислением с помощью четырехокиси осмия до глицеринового производного. При отщеплении воды образуется дезоксикортикостерон; еще лучше ацетилированный продукт путем перегонки с цинковой пылью превращать в дезоксикортикостерон-ацетат;
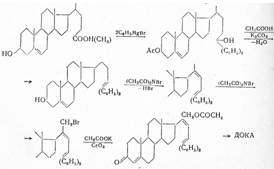
Практическое значение имеет использование Зβ-окси-5-холеновой кислоты (I), получаемой в качестве побочного продукта при окислении холестерилацетатдибромида. После превращения ее в метиловый эфир и действия 2 мол магний-бром-фенила получают соответствующий третичный спирт, который ацетилируют. При отщеплении воды кипячением с уксусной кислотой и дезацетилировании с помощью поташа вторичная спиртовая группа при С3 окисляется по Оппенауэру и бромированием с помощью N-бромсукцинимида, а также последующим отщеплением бромистого водорода с помощью диметиланилина получают диен. При дальнейшем действии N-бромсукцинимида на свету образуется 21-бромпроизводное, от которого боковую цепь отщепляют хромовой кислотой после предварительного ацетилирования:
В дальнейших, технически важных синтезах в качестве исходного продукта использовали 5-прегнен-3-β-ол-20-онацетат. При обработке его тетраацетатом свинца образуется 21-ацетоксипроизводное, которое при действии раствора гидрокарбоната калия селективно деацетилируется у С21 и полученное соединение с помощью хлористого тнонила превращают в С21-хлорид, а при дезацетилировании при С3 и окислении по Оппенауэру — в 21-хлорпрогестерон. При взаимодействии последнего с ацетатом натрия образуется дезоксикортикостерон-ацетат:
Дезоксикортикостерон-ацетат — белый или белый с кремовым оттенком кристаллический порошок без запаха, т. пл. 154—160°. Растворим в хлороформе, ацетоне, диоксане и спирте, не растворим в воде. Вращает плоскость поляризации вправо. Удельный показатель поглощения 430 (с = 0,001, 95%-ный спирт) при 240 ммк. Восстанавливает аммиачный раствор нитрата серебра и окрашивается концентрированной серной кислотой; при прибавлении хлороформа последний окрашивается в оранжевый цвет с красной флуоресценцией, водный слой окрашивается в зеленоватый цвет. Чистоту препарата определяют по отсутствию сульфатной золы и потере в весе (допускается потеря при высушивании до постоянного веса при 100—105° не более 0,5%). Хранят с предосторожностью (список Б), в банках оранжевого стекла с притертыми пробками, в сухом месте. Высшая разовая доза — 0,01 г, суточная — 0,02 г. Применяют при болезни Аддисона, общей мышечной слабости и других заболеваниях внутримышечно в масляных растворах по 5 мг 3 раза в неделю до 10 мг ежедневно. Препарат вызывает задержку ионов натрия и повышение выделения калия; противопоказан при гипертонической болезни, сердечной недостаточности, атеросклерозе и др.
|