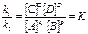Дәріс тақырыбы: Аналитикалық химияның әдістері мен анализ түрлері. Анализдің түрлері.
Дәріс тезистері:Химиялық анализді негізгі сатылары. Анализ әдісін таңдау және анализ сызбасын құру. Абсолютті (эталонсыз) және салыстырмалы анализ әдістері. Метрологиялық негізі түсініктер мен ұғымдары: өлшеу, өлшеу әдістері мен тәсілдері, өлшеу нәтижелерге қойылатын метрологиялық талаптар, өлшеу нәтижелердің сенімділігін қамтамасыз етудің әдістері мен негізгі принциптері, ауытқулар. Аналитикалық белгі және кедергілер. Аналитикалық белгідегі ақпарат мөлшері. Анализ әдістерінің негізгі сипаттамалары: дұрыстығы мен қайталанғыштылығы, сезілмалдық коэффициенті, анықтау шегі, анықталатын құрамының үстінгі мен астыңғы шектері. Анализ ауытқуларының жіктелуі. Жүйелі мен кездейсоқ ауытқулар. Химиялық анализдің кейбір сатыларының ауытқулары. Нақтылықты бағалау әдістері: стандартты үлгілерді қолдану, қоспалар әдісі, өлшендіні түрлену әдістері, басқа әдістерме салыстыру. Стандартты үлгілер, оларды дайындау, аттестация және қолдану. Өлшеу нәтижелерінің статистикалық өңдеуі. Градуирленген графиктарды құрудағы ең кіші квадраттар әдісін қолдану. Тапта келістілігі; татпа мен анализ объекті; татпа мен анализ әдісі. Келісті татпаны іріктеу әдісін мен мөлшерін шарттайтын факторлар. Гомогенді мен гетерогенді құрамды татпаларды алу. Берілген анализ үшін татпаны қажетті түрге айналдырудың негізгі тәсілдері: әртүрлі орталарда еріту; пісіру, балқыту, жоғары температура, қысым, жоғарыжиілікті разряд әсерінен ыдырату; әртүрлі тәсілдері қиыстыра қолдану; органикалық қосылыстарыны ыдырау ерекшеліктері. Татпа дайындау кезінде компоненттердің жоғалуы және кірленуді есептеу мен болдырмау әдістері. Сапалық анализдегі катиондар мен аниондарды Ышқыл-негіздік жүйе бойынша топтастыру
Негізгі [1-3], Қосымша [4-11]. Мерзімдік әдебиеттер [12-14] Электрондық оқулықтар мен оқу құралдары [15-16] Интернет көздері [17-20]
Дәріс тақырыбы: Массалар әрекеттесу заңы. Тура және кері реакциялар. Дәріс тезистері:Аналитикалық химия үшін химиялық реакцияның жылдамдығына реакцияға түсетін заттардың концентрациясының әсерін қарастыру қажет. Ол МӘЗ –мен анықталады.Химиялық тепе-теңдік жағдайында реакция өнімінің стехиометриялық коэффициентіне сәйкес дәрежесіндегі активтіліктерінің көбейтіндісі бастапқы заттардың активтіліктерінің көбейтіндісіне қатынасы берілген температура, қысымда және берілген еріткіште тұрақты шама. Химиялық реакцияның жылдамдығы реакцияласушы заттардың концентрациясының стехиометриялық дәрежесіне шығарылған көбейтіндісіне тура пропорционал. МӘЗ ең алғаш Норвегия ғалымдары Гульдберг пен Вааге және орыс ғалымы Бекетов ұсынды. аА + вВ ↔ сС + dD Vn = k1 [A]a [B]в, Vo= k2 [C]c [D]d
k –реакция жылдамдығының константасы, Vn-тура, Vo- кері реакциялардың жылдамдықтары. Егер Vn = Vo, яғни k1 [A]a [B]в = k2 [C]c [D]d /: k2 [A]a [B]в
Мұндағы: К – химиялық тепе –теңдіктің концентрациялық константасы. Негізгі [1-3], Қосымша [4-11]. Мерзімдік әдебиеттер [12-14] Электрондық оқулықтар мен оқу құралдары [15-16] Интернет көздері [17-20]
|