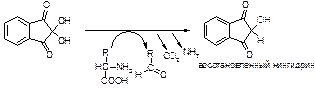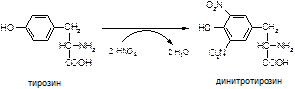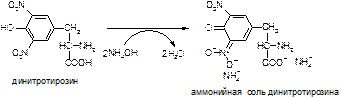Состав и свойства белков
РАБОТА 1. ЦВЕТНЫЕ РЕАКЦИИ НА БЕЛКИ Цель работы: ознакомиться с основными наиболее распространён-ными цветными реакциями на белки и доказать, что с их помощью можно выявить сходство и различия в аминокислотном составе исследуемых белков (на примере яичного альбумина и желатина). Задачи: · провести цветные реакции на белки с раствором яичного альбумина и желатина; · определить, какой из исследуемых белков является полноценным; · отметить, какие из проведённых реакций являются универсальными, а какие – специфическими; · сравнить результаты проведённых исследований и сделать выводы. Цветные реакции на белки являются качественными реакциями, обусловленными специфическими группами – радикалами. Некоторые из таких реакций широко используются в биохимической практике для изучения структуры и аминокислотного состава белков, их количественного определения.
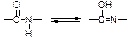
1. Биуретовая реакция (на обнаружение пептидных связей в белках) Принцип метода. Белки (пептиды) в щелочном растворе в присутствии солей меди (II) образуют комплексные её соединения, окрашенные в сине-фиолетовый или красно-фиолетовый цвет. Для пептидной (амидной) группы характерна лактам-лактимная таутомерия:
В щелочной среде преобладающая лактимная (енольная) форма полипептида взаимодействует с гидроксидом меди (II) с образованием стабильного окрашенного комплекса:
Ход работы. К 1 мл 1%-го раствора белка добавляют 1 мл 10%-го раствора щёлочи (NaOH или KOH) и 1 каплю 1%-го раствора сульфата меди. Появляется сине-фиолетовое или красно-фиолетовое окрашивание. 2. Нингидриновая реакция (на аминогруппу, находящуюся в α-положении) Принцип метода. Белки, полипептиды и свободные a-амино-кислоты при нагревании реагируют с нингидрином (трикетогидрин-ден-гидратом) с образованием продукта конденсации, окрашенного в фиолетовый цвет:
Ход работы. К 1 мл 1%-го раствора белка прибавляют 0,5 мл 0,5%-го раствора нингидрина и нагревают до кипения. Появляется сине-фиолетовое окрашивание. 3. Реакция Сакагучи (на аргинин) Принцип метода. Белки, содержащие аргинин, в присутствии щелочи дают красное окрашивание с гипобромитом и a-нафтолом. Гуанидиновая группа аргинина окисляется гипобромитом, и окисленный аргинин при взаимодействии с a-нафтолом образует продукт конденсации красного цвета:
Ход работы. К 0,5 мл 1%-го раствора белка добавляют 0,5 мл 10%-го раствора щелочи, 3 капли 0,1%-го спиртового раствора a-нафтола и после перемешивания – 2-3 капли 2%-го раствора гипобромита натрия. Появляется красное окрашивание.
4. Реакция Фоля (на цистеин и цистин) Принцип метода. При кипячении белка со щёлочью от цистеина (цистина) легко отщепляется сера в виде сероводорода, который в щелочной среде образует сульфид натрия:
Для выявления сульфида натрия используют ацетат свинца, который при взаимодействии с гидроксидом натрия превращается в тетрагидроксоплюмбат натрия: Pb(CH3COO)2 + 4NaOH ® Na2[Pb(OH)4]+ 2CH3COONa. В результате взаимодействия ионов серы и свинца образуется сульфид свинца чёрного или бурого цвета: Na2S + Na2[Pb(OH)4] ® PbS¯ + 4NaOH. Ход работы. К 1 мл 1%-го раствора белка или кусочку шерстяной нити добавляют 1 мл 30%-й щёлочи и 3-4 капли 5%-го раствора ацетата свинца. При интенсивном кипячении жидкость окрашивается в бурый или чёрный цвет. 5. Ксантопротеиновая реакция (на ароматические аминокислоты) Принцип метода. При нагревании с концентрированной азотной кислотой белки дают жёлтое окрашивание. Реакция обусловлена наличием в белках ароматических аминокислот (фенилаланина, тирозина и триптофана) и основана на образовании нитропроизводных этих аминокислот, имеющих жёлтую окраску:
Нитропроизводные аминокислот в щелочной среде образуют соли хиноидной структуры, окрашенные в оранжевый цвет:
Ход работы. К 1 мл 1%-го раствора альбумина или яичного белка добавляют 5 капель концентрированной азотной кислоты. Появляется осадок. При осторожном нагревании смесь окрашивается в жёлтый цвет. После охлаждения осторожно добавляют 10 капель концентрированного раствора аммиака (или 30%-й раствор едкого натра), при этом жёлтая окраска переходит в оранжевую. Проделывают эту реакцию с 1%-м раствором желатина, сравнивают результаты и делают выводы.
6. Реакция Милона (на тирозин) Принцип метода. Реакция Милона открывает в белке тирозин, в составе которого имеется фенольный гидроксил. При нагревании белка с реактивом Милона (смесь нитратов и нитритов ртути (I) и (II), растворённых в концентрированной азотной кислоте) образуется осадок, окрашенный сначала в розовый, а затем в красный цвет. Реактив Милона даёт окрашивание почти со всеми фенолами:
Ход работы. К 1 мл 1%-го раствора яичного белка добавляют 3-5 капель реактива Милона и осторожно нагревают до образования окрашенного в красный цвет осадка. Аналогично проделывают реакцию с растворами желатина. Полученные результаты сравнивают и делают вывод.
7. Реакция Паули (на гистидин и тирозин) Принцип метода. Реакция Паули позволяет обнаружить в белке аминокислоты гистидин и тирозин, которые образуют с диазобензолсульфокислотой соединения вишнёво-красного цвета. Диазобензолсульфокислота образуется в реакции диазотирования при взаимодействии сульфаниловой кислоты с нитритом натрия (или калия) в кислой среде:
Ход работы. К 1 мл 1%-го раствора сульфаниловой кислоты (готовится на 5%-м растворе соляной кислоты) прибавляют 2 мл 0,5%-го раствора нитрита натрия, тщательно перемешивают, добавляют 2 мл 1%-го раствора яичного белка и после перемешивания 6 мл 10%-го раствора карбоната натрия. После перемешивания смесь окрашивается в вишнёво-красный цвет. Реакцию проделывают с яичным альбумином и желатином, сравнивают полученные результаты и делают вывод.
Выводы:
|