Виконання роботи. У колбу об’ємом 500 мл відмірюють точно 104 мл розчину сульфатної кислоти з молярною концентрацією еквівалентів 0,05 моль/л
У колбу об’ємом 500 мл відмірюють точно 104 мл розчину сульфатної кислоти з молярною концентрацією еквівалентів 0,05 моль/л, доводять до мітки водою і перемішують. Такий розчин містить 0,5 мг йонів SO42- у 1 мл. Цей розчин служить вихідним (еталонним) для готування стандартного розчину. У дві мірні колби об’ємом 100 мл поміщають по 2 мл розчину барій хлориду, розбавляють трохи водою і додають по 3 мл розчину з масовою часткою желатину 0,4 %. Потім при перемішуванні в одну з колб, у якій буде знаходитися стандартний розчин, уводять таку кількість сульфатної кислоти, щоб у ній утримувався 1 мг йонів SO42-. Одночасно в іншу колбу з досліджуваним розчином добавляють довільну (але відому) кількість йонів SO42-. Об’єм обох розчинів швидко доводять до мітки і вміст колб старанно перемішують. Через 3-5 хвилин розчини переносять у кювети нефелометра (30 мм) і проводять виміри. Якщо похибка виміру не перевищує 2 %, одержують у викладача контрольні розчини і визначають їхню концентрацію. Робота з фотометром ЛМФ-72 1. Для переключення приладу в режим нефелометрії перемикач "род работы" і ручку переключення кювет витягають на себе до упора. 2. Включають прилад у мережу. Натискують кнопку "сеть" і "расширитель". Прилад прогрівається 30 хвилин. 3. Ручку “чувствительность” (грубо, точно) обертанням проти годинної стрілки встановлюють у нульове положення (до упора). 4. Для виміру використовують 3 прямокутні кювети. 5. Кювети заливають розчином до риски, беруть кювети за верхні кути, стінки кювет старанно протирають фільтрувальним папером. 6. У кюветне відділення вміщують кювету з дистильованою водою. Ручкою "установка 0" (грубо, точно) стрілку приладу сполучають із "0" шкали. 7. Вміщують у кюветну камеру кювету зі стандартним розчином і обертанням ручки "установка 100" проти годинникової стрілки і "чутливість" (грубо, точно) по годинниковій стрілці сполучають стрілку приладу з кінцевою точкою шкали (100). 8. Операції 6, 7 повторюють 3 - 4 рази до одержання сталого показника "0" і "100". Щораз, замінюючи кювету у кюветній камері, необхідно почекати 2 хвилини, а потім знімати показання приладу. 9. У кювету 3 заливають досліджуваний розчин, поміщають її в прилад і знімають показання по шкалі. 10. Розраховують концентрацію досліджуваного розчину стосовно стандартного, прийнявши концентрацію стандартного за 100. 11. По закінченні вимірів кювети промивають, протирають зсередини фільтрувальним папером. Прилад вимикають із мережі. 12. Дані заносять у таблицю 8. Таблиця 8 Результати визначення йонів SO42–
За результатами роботи зробити висновок. _______________________________ ________________________________________________________________________________________________________________________
Питання та вправи для самоконтролю 1. Наведіть основний закон світлорозсіяння (рівняння Релея) і охарактеризуйте величини, які входять до нього. 2. Які умови треба дотримувати для забезпечення достатньої точності нефелометричних вимірювань? 3. Як пов’язана інтенсивність світла, яке пройшло через суспензію, з концентрацією речовини, що аналізується, в турбідиметричному методі? 4. Назвіть переваги та недоліки методів нефелометрії та турбідиметрії? 5. Чим відрізняються між собою нефелометрія і турбідиметрія. 6. Які прилади використовують при нефелометричних вимірюваннях? Наведіть оптичну схему нефелометра. 7. При визначенні натрій хлориду у розчині натрій гідроксиду приготували серію стандартних розчинів. Для цього V мл розчину NaCl (T = 0,100 мг/мл) перенесли у мірні колби місткістю 25,0 мл, додали реактиви, які необхідні для одержання суспензії AgCl, виміряли удавані оптичні густини за допомогою нефелометра і одержали значення: V, мл 0,30 0,50 0,80 1,50 Dудавана 0,670 0,550 0,390 1,150. Наважку розчину, що аналізується, масою 21,74 г нейтралізували нітратною кислотою, перенесли у мірну колбу і приготували 50,0 мл розчину, 2,0 мл якого використали для приготування 25,0 мл суспензії AgCl. Визначити масову частку NaCl, якщо удавана оптична густина суспензії AgCl має значення 0,480.
2.3. Емісійна фотометрія Люмінесцентні методи аналізу Емісійна фотометрія базується на вимірі енергії, що випромінюється речовиною внаслідок енергетично збудженого стана. До методів емісійної фотометрії відносять люмінесценцією, яка заснована на ефекті енергетичного збудження молекул і атомів досліджуваної речовини, як наслідок впливу жорсткого ультрафіолетового випромінювання, і полум'яну фотометрію,яка заснована на ефекті енергетичного збудження полум'ям структурних складових досліджуваної речовини. Люмінесцентні методи аналізу засновані на спроможності деяких речовин виділяти променисту енергію під впливом електромагнітного випромінювання з більш короткою довжиною хвилі. Це явище називається фотолюмінесценцією. Якщо розташувати по лінії хвиль спектральну характеристику збудливої системи і смугу люмінесценції, то одержимо графік, зображений на рис.11.
g - квантовий вихід люмінесценції: g = Флуориметрія заснована на вимірі інтенсивності флуоресценції речовин. Інтенсивність флуоресценції залежить від концентрації речовини. Звичайно для флуориметричних вимірів застосовують концентрації речовин 10–4-10–6 г/мл; в цих межах залежність інтенсивності від концентрації прямолінійна. Кількісні виміри у флуориметрії засновані на використанні стандартних розчинів речовин (спосіб порівняння або калібрувального графіку). Якщо в якості розчину порівняння застосовується стандартний розчин речовини, то концентрацію досліджуваного розчину (Сх) розраховують за формулою: Лабораторна робота № 4 Люмінесцентний метод визначення замаслювачів у тканинах Мета роботи: визначити масову частку (відсотковий вміст) замаслювача на тканині. Обладнання і реактиви: джерело ультрафіолетового випромінювання зі світлофільтром, пробірки, що нелюмінесціюють, мірний пальчик, піпетки на 1 мл, бавовняна тканина, ваги аналітичні, розчинник – тетрахлорокарбон (чотирьох-хлористий вуглець CCl4).
|


 . Чим більше g, тим інтенсивніше люмінесценція. Як правило g < 1. Проста модифікація кількісного люмінесцентного аналізу - метод стандартних серій.
. Чим більше g, тим інтенсивніше люмінесценція. Як правило g < 1. Проста модифікація кількісного люмінесцентного аналізу - метод стандартних серій. , де
, де  ,
, 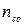 ,
,  –відповідно показання флуориметру для досліджуваного розчину, стандартного розчину, контрольного розчину;
–відповідно показання флуориметру для досліджуваного розчину, стандартного розчину, контрольного розчину;  – концентрація стандартного розчину.
– концентрація стандартного розчину.


