Адсорбция
Адсорбцией называется явление сгущения газообразного или растворенного вещества на поверхности раздела фаз. Подробно адсорбция изучается в курсе коллоидной химии. Здесь будут изложены лишь элементы соответствующих представлений. Начнем с определений. Более плотная фаза (жидкость или твердое тело, на поверхности которых происходит адсорбция) называется адсорбентом. Менее плотная фаза (газ, растворенное вещество, которое адсорбируется на поверхности адсорбента) называется адсорбтивом. Адсорбент с адсорбированным на нем адсорбтивом называется адсорбатом. Весьма грубо силы, действующие между молекулами адсорбтива и поверхностью адсорбента, можно разделить на силы Ван-дер-Ваальсовы (слабые) и силы химические (сильные). Ван-дер-Ваальсовым силам соответствуют энергии типа потенциальной энергии Леннард–Джонса, а химическим силам — энергии химической связи. Важнейшей характеристикой адсорбции является поверхностная концентрация адсорбтива α — количество адсорбтива (адсорбированного вещества), приходящееся на единицу площади поверхности адсорбента α = ν/ S; [α] = моль/м2. Простейшая теория адсорбции была создана Ирвингом Ленгмюром. Эта теория основана на представлении о существовании на поверхности адсорбента «активных центров». Активными центрами называются малые области на поверхности, такие, что молекулы адсорбента из этих областей легче связываются с молекулами адсорбтива. Конечно, в таком определении часто бывает элемент тавтологии. Действительно, на вопрос: «Что такое эти малые области?» ответ будет: «Это активные центры». Сам Ленгмюр представлял, что активные центры — это возвышенности, пики на адсорбирующей поверхности. С примитивной точки зрения в активных центрах усиливается электрическое поле, сгущаются линии напряженности вокруг острия. Представление об активных центрах приводит к заключению, что α ≤ αmax, где αmax — поверхностная концентрация адсорбтива, при которой все активные центры заняты. С другой стороны, если считать, что с одним активным центром связывается одна молекула адсорбтива (мономолекулярная теория адсорбции), то α определяется давлением (парциальным давлением) р. Ведь именно давление в идеальном газе определяется числом молекул, пришедших (столкнувшихся) к поверхности в единицу времени. В результате Ленгмюр предложил уравнение изотермы адсорбции в виде (закон Ленгмюра):
Величина 1/ А называется константой равновесия. Само А и, соответственно, 1/ А не зависят от поверхностной концентрации α.
|

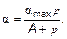 (5.5)
(5.5)


