Процессы испарения и конденсации
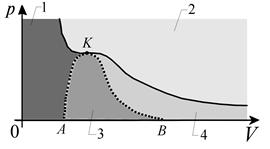
Испарение, как явление, состоит в том, что молекулы жидкости покидают ее поверхность. Покидающие жидкость молекулы преодолевают притяжение соседних молекул и совершают работу против этих сил притяжения. Эта работа называется работой выхода испарения. Вышедшие из жидкости молекулы образуют газ, который называется паром. Выходящие молекулы совершают работу против сил внешнего давления, связанную с увеличением объема при переходе в газообразное состояние. Совершить работу выхода и преодолеть силы внешнего давления способны только молекулы с энергией больше средней. Из-за этого, при испарении, средняя энергия молекул жидкости понижается и, в силу основного уравнения молекулярно-кинетической теории Явление перехода молекул пара обратно в жидкость называется конденсацией. Очевидно, что чем больше плотность пара, тем большее количество молекул возвращается в жидкость. Если число испаряющихся молекул за достаточно длительное время равно числу конденсирующихся молекул, то пар называется насыщенным. Зависимость давления от объема для систем с двумя и более фазами вещества называется фазовой диаграммой. Фазовая диаграмма «жидкость–пар–газ»приведена на рис. 5.4.
Рис. 5.4. Диаграмма равновесных состояний: жидкость (1) — газ (2) — жидкость и насыщенный пар (3) — ненасыщенный пар (4)
|

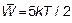 (см. гл. 1), понижается также и температура жидкости.
(см. гл. 1), понижается также и температура жидкости.