Сублимация (испарение)
Наиболее радикальное, полное, изменение симметрии наблюдается при переходе из твердого состояния в газообразное. Действительно, твердое тело характеризуется наибольшей степенью симметрии, а газу соответствует полное отсутствие симметрии, выраженное в хаотическом расположении молекул. Переход вещества из кристаллического состояния непосредственно (без плавления) в газообразное называется сублимацией. Сублимация очень похожа на испарение. И при сублимации, и при испарении объем, приходящийся на одну молекулу в газообразной фазе (паре) V 2, гораздо больше объема на молекулу в другой (твердой или жидкой) V 1 << V 2. Поэтому в формуле Клапейрона–Клаузиуса объемом V 1можно пренебречь. Тогда эта формула запишется как dр / dT = q / TV 2. Рассматривая пар как идеальный газ, выразим его объем V = V 2 N через давление и температуру: V 2 = kT / р (k — постоянная Больцмана). Формула Клапейрона–Клаузиуса для испарения(сублимации)имеет вид:
Интегрируя, найдем, что dр / р превратится в ln р, а dT / T 2в (– Т –1). Отсюда следует, что если теплоту фазового перехода q можно считать независящей от температуры, то давление насыщенного пара при сублимации (испарении) меняется с температурой по экспоненциальному закону:
где ln C — постоянная интегрирования. Эта формула является частным случаем распределения Больцмана. Теплота q, конечно, может быть выражена через молярную qNA или удельную L = qNA / M теплоту сублимации(испарения). Теплоты сублимации, как удельная, так и молярная, являются характеристиками вещества и собраны в справочные таблицы.
|

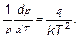 (5.26)
(5.26) (5.27)
(5.27)


