ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
195. Исходя из степени окисления хлора в соединениях HCl, HClO3, HClO4 определить, какое из них является только окислителем, только восстановителем и какое может проявлять как окислительные, так и восстановительные свойства 196. На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме: 197. На основании метода электронного баланса расставьте коэффициенты в уравнении реакции, идущей по схеме: 198. Методом электронного баланса расставить коэффициенты в следующих уравнениях реакций:
205. Окисление или восстановление происходит при переходах:
199. Указать окислитель, восстановитель и подобрать коэффициенты уравнения:
200. Определить степень окисления кислорода в соединениях: ClO2, F2O, H2O, H2O2, CaO, CaO2, PbO, PbO2, хрома в соединениях: Cr2(SO4)3, K2Cr2O7, CrO2Cl2, KCrO2, K2CrO4, CrO3 и хлора в соединениях: Cl2, NaOCl, CaOCl2, AlCl3, HСlO4, NaClO2, Cl2O7. Окислительные или восстановительные свойства проявляют эти соединения? 201. Исходя из степени окисления фосфора в соединениях PH3, H3PO4, H3PO3 определить, какое из них является только окислителем, только восстановителем и какое может проявлять и окислительные, и восстановительные свойства. На основании метода электронного баланса расставить коэффициенты в уравнении реакции, протекающей по схеме:
202. Исходя из степени окисления хрома, иода и серы в соединениях K2Cr2O7, KJ, H2SO3 определить, какое из них является только окислителем, только восстановителем и какое может проявлять и окислительные, и восстановительные свойства. На основании метода электронного баланса расставить коэффициенты в уравнении реакции, идущей по схеме:
203. Составьте электронные уравнения и укажите, какой процесс – окисление или восстановление – происходит при следующих превращениях: 204. Реакции выражаются схемами:
Составить электронные уравнения, указать, какое вещество является окислителем и восстановителем и расставить коэффициенты. 205. Реакции выражаются схемами:
Составить электронные уравнения, указать, какое вещество является окислителем и восстановителем и расставить коэффициенты. 206. Указать окислитель, восстановитель и подобрать коэффициенты уравнения:
207. Методом электронного баланса расставить коэффициенты в следующих уравнениях реакций:
208. Реакции выражаются схемами:
Составить электронные уравнения, указать, какое вещество является окислителем и восстановителем и расставить коэффициенты. 209. Реакции выражаются схемами: P+HNO3+H2O®H3PO4+NO K2S+KMnO4+H2SO4®S+K2SO4+MnSO4+H2O.. Составьте электронные уравнения, расставьте коэффициенты. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем; какое вещество окисляется, какое восстанавливается. 210.Реакции выражаются схемами: HNO3+Ca®NH4NO3+Ca(NO3)2+H2O; KMnO4+Na2SO3+KOH®K2MnO4+Na2SO4+H2O. Составьте электронные уравнения, расставьте коэффициенты. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем; какое вещество окисляется, какое восстанавливается. 211.Реакции выражаются схемами: K2Cr2O7 +H2S+H2SO4®S+Cr2(SO4)3+K2SO4+H2O KMnO4+HBr®Br2+KBr+MnBr2+H2O.. Составьте электронные уравнения, расставьте коэффициенты. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем; какое вещество окисляется, какое восстанавливается. 219.Реакции выражаются схемами: H3AsO3 +KMnO4+H2SO4®H3AsO4+MnSO4+K2SO4+H2O; Н2S+Cl2+H2O®H2SO4+HCl. Составьте электронные уравнения, расставьте коэффициенты. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем; какое вещество окисляется, какое восстанавливается. 212.Реакции выражаются схемами: KClO3+Na2SO3®KCl+Na2SO4; P+HClO3+H2O®H3PO4+HCl. Составьте электронные уравнения, расставьте коэффициенты. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем; какое вещество окисляется, какое восстанавливается.
|

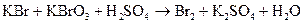 .
. .
.
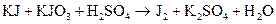
 .
.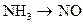 для азота,
для азота,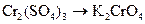 для хрома,
для хрома,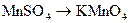 для марганца,
для марганца, для марганца.
для марганца.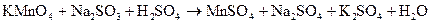

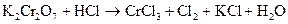
 .
.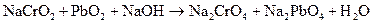 .
. ;
; 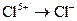 ;
;  . На основании метода электронного баланса расставьте коэффициенты в уравнении реакции, идущей по схеме:
. На основании метода электронного баланса расставьте коэффициенты в уравнении реакции, идущей по схеме:  .
.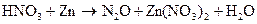


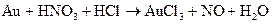 .
.








