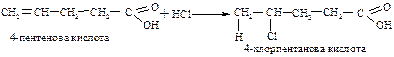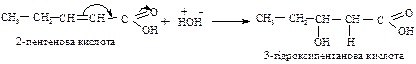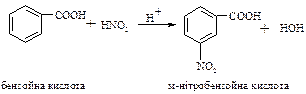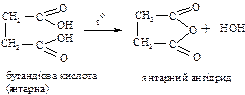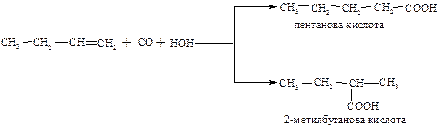б) ненасичені кислоти
Ненасичені кислоти містять подвійний або потрійний зв’язки між вуглецевими атомами і вступають у реакції ненасичених сполук (приєднання, полімеризації, окислення): реакція приєднання:
У кислотах, у яких подвійний зв’язок знаходиться у α,β-вуглецевих атомів спостерігається спряження між π-електронами С = С і π-електронами С = О зв’язків (+М) і водень приєднується до вуглецю з більшою електроною густиною:
в) ароматичні кислоти Кабоксильна група – замісник ІІ рода, тому заміщення відбувається в мета-положення:
Особливості двохосновних (дикарбонових) кислот Наявність двох карбоксильних груп, їх взаємне положення в молекулі надає цім кислотам особливих властивостей, які виявляються наприклад, при нагріванні.
При нагріванні двоосновних кислот, які в головному ланцюзі містять до трьох вуглецевих атомів, відщеплюється СО2 і утворюються одноосновні кислоти (реакція декарбоксилювання):
Якщо в головному ланцюзі більше трьох вуглеців, то при нагріванні утворюються внутрішні циклічні ангідриди:
Окремі представники та їх застосування Багато органічних кислот: мурашина, оцтова, пропіонова, масляна, стеаринова (С17Н35СООН), олеінова (С17Н33СООН), бензойна, щавлева та інші містяться у різноманітної рослинної та тваринної сировині. Деякі з них використовують у харчовій промисловості. Так, мурашину кислоту застосовують для консервування соків і білково-вітамінних концентратів, для дезинфекції чанів для бродіння при виробництві спирту, пива і т.д. оцтову кислоту використовують як смакову і консервуючу речовину. Сорбінова (2, 4-гексадієнова) і бензойна кислоти використовуються для консервування м’ясних і рибних виробів, сира, фруктових компотів, овочів та ін.
|