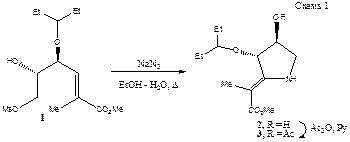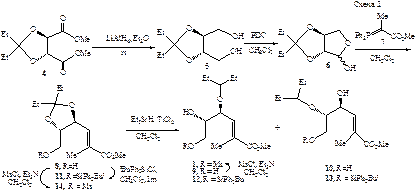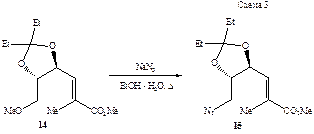ТЕРПЕНСУЛЬФИДЫ НА ОСНОВЕ (R)-4-МЕНТЕН-3-ОНА
Тухватшин В.С.,1 Смольников А.А.2
1 Башкирский государственный университет, Уфа, Россия. Аспирант 3г. vadimtukhvatshin@yandex.ru 2 Башкирский государственный университет, Уфа, Россия. Студент VI курса. Научные руководители: Латыпова Э.Р., Ишмуратов Г.Ю., Муслухов Р.Р.
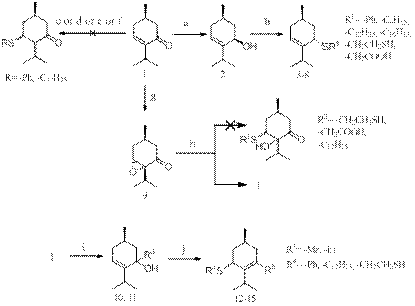
Известно [1], что введение в молекулу природных монотерпеноидов [(+)-3-карена, (+)- цис- вербенола, (-)-карвона, β-пинена, (+)-лимонена и др.] одной или нескольких сульфидных групп ведет к увеличению эффективности биологического действия. Поэтому с целью расширения круга потенциально биологически и фармакологически активных терпенсульфидов нами выполнены превращения доступного из L-ментола оптически чистого (R)-4-ментен-3-она 1 и его производных [ненасыщенных спиртов 2, 10, 11 и эпоксида 9 ] в направлении соединений данной группы 3 - 8, 12 - 15.
Реагенты: a) NaBH4, EtOH, -780C; b) R1SH, ZnCl2, CH2Cl2, rt; c) RSH, K2CO3, Me2CO, rt; d) RSH, K2CO3, Me2CO, 55-60°C; e) RSH, BF3·OEt2(kat.), CH2Cl2, rt; f) RSH, BF3·OEt2(eq.), CH2Cl2, rt.; g) NaOH, H2O2, rt.; h) R2SH, EtONa, 80°C; i) R3Li, Et2O, -780C; j) R4SH, ZnCl2, CH2Cl2, rt.
Литература: [1] E.V. Sirazieva, V.А. Startseva, L.Е. Nikitina, S.А. Lisovskaja, N.I. Glushko, Abstracts of International Conference «Organic chemistry since Butlerov and Beilstein until present»,St. Petersburg, 447, (2006) ГЕТЕРОЦИКЛИЗАЦИЯ 5-(МЕТОКСИКАРБОНИЛ)-2-ГИДРОКСИ-3-(ПЕНТ-3-ИЛОКСИ)-ГЕКС-4-ЕНИЛ МЕТАНСУЛЬФОНАТА В РЕАКЦИИ С NaN3
Фаткуллина И.И.,1 Халикова Г.М.2,Егоров В.А.3
1 Башкирский государственный университет, Уфа, Россия. Студент V курса. fangim@anrb.ru 2 Башкирский государственный университет, Уфа, Россия. Аспирант 3г. 3 Институт органической химии Уфимского научного центра РАН, Уфа, Россия. Молодой учёный. Научный руководитель: д.х.н., проф. Гималова Ф.А. (ИОХ УНЦ РАН)
В ходе разработки синтеза новых модификатов известного антивирусного средства Тамифлю [1,2] на стадии введения в структуру соединения 1 аминной функции реакцией замещения Ms-группы NaN3 мы наблюдали интересную нетривиальную реакцию образования производного пирролидина 2.
На схеме 2 показан синтез соединения 1. Полученный из L-винной кислоты кеталь 4 восстановили LiAlH4 до диола 5.
Следующая реакция окисления 5 PDC достаточно селективна и останавливается на стадии образования ацеталя 6, который стереоселективно реагирует с фосфораном 7, давая α,β-непредельный эфир 8. Стадия восстановительного раскрытия кетальной функции 8 системой Et3SiH–TiCl4 [3] привела к диолам 9 и 10 в соотношении ~3:2. Селективность на этой стадии удалось несколько улучшить введением в эту реакцию Si-производного 11, при этом спирты 12 и 13 образовались в соотношении 2:1. Мезилирование диола 9 протекает региоселективно, при этом с высоким выходом образуется использованный в работе первичный мезилат 1. Позже был найден более эффективный путь синтеза соединения 1 из мезилата 14: при раскрытии диоксоланового цикла 14 с помощью Et3SiH–TiCl4 наблюдалось образование лишь соединения 1. В отличие от соединения 1, мезилат 14 в реакции с NaN3 дает ожидаемый азид 15.
Работа выполнена при финансовой поддержке программы РФФИ-Поволжье (проект 11-03-97013 р_а). Литература: [1] Shibasaki M., Kanai M. Eur. J. Org. Chem. 1839 (2008). [2] Magano J. Chem. Rev. 109, 4398 (2009). [3] Mori A., Ishihara K., Yamamoto H. Tetrahedron Lett. 27, 987 (1986).
|