ХИМИЯ р-ЭЛЕМЕНТОВ III ГРУППЫ
В В Е Д Е Н И Е В настоящем пособии обобщены и систематизированы сведения по химии элементов III и IV групп периодической системы Д.И. Менделеева. Данный раздел является частью курса “Общая и неорганическая химия”. Удобная форма изложения материала (в виде таблиц и схем с необходимыми пояснениями) способствует его лучшему изучению и закреплению. Структура построения разделов пособия по свойствам p- и d-элементов одинакова: краткая общая характеристика подгруппы, сведения о простых веществах, водородных соединениях, соединениях с кислородом, бинарных соединениях, гидроксидах, солях. Умение решать задачи по химии является основным критерием творческого подхода к изучаемому предмету, поэтому пособие содержит 40 вариантов заданий по свойствам p- и d-элементов III и IV групп. Получение полноценных знаний по химии основано на конкретном изучении свойств веществ и их превращений, чему способствует выполнение лабораторных работ. В данном учебном пособии предложена лабораторная работа, которая включает опыты, отражающие свойства элементов III и IV групп и их соединений. Материал пособия – необходимое дополнение к основной литературе по неорганической химии, способствующее более глубокому изучению предмета.
ХИМИЯ р-ЭЛЕМЕНТОВ III ГРУППЫ
К р-элементам (главная подгруппа) III группы относятся два распространенных элемента - бор и алюминий, и три редких - галлий, индий и таллий. С увеличением атомного номера элементов энергия ионизации атомов уменьшается, увеличиваются металлические свойства: бор − неметалл, остальные элементы − металлы. В таблицах 1-3 приведены важнейшие данные о р - элементах III группы.
Таблица 1 Общие сведения
Таблица 2 Атомные характеристики элементов
Таблица 3 Основные физико-химические свойства
1.1. Способы получения Технический бор получают из природного сырья в несколько стадий: Na2B4O7∙10H2O Чистый бор получают электролизом расплавленных фтороборатов, восстановлением или разложением его галогенидов, а также разложением гидридов бора: 2BBr3 + 3H2 = 2B + 6HBr B2H6 = 2B + 3H2 Алюминий получают электролизом глинозема (Al2O3) в расплавленном криолите Na3AlF6 в присутствии флюсов AlF3, CaF2, MgF2. Ga, In и Tl получают при переработке полиметаллических руд. При этом данные элементы выделяют в виде оксидов или хлоридов, которые затем химическим или электрохимическим способом восстанавливают до металлов.
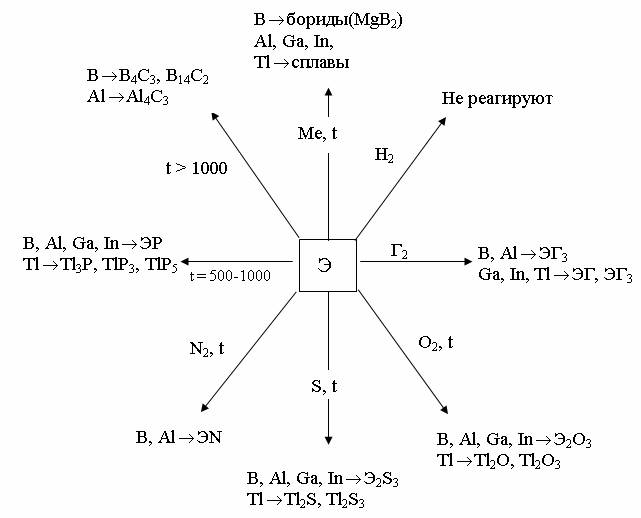
1.2. Химические свойства Бор – неметалл, остальные элементы – металлы. Все элементы проявляют степень окисления +3, а бор может быть отрицателен (–3). Для таллия наиболее характерна степень окисления +1. Химия бора во многом напоминает химию кремния (правило диагонали); они близки по электроотрицательности, их гидроксиды являются слабыми кислотами, оксиды имеют высокие температуры плавления и очень устойчивы, соединения с металлами тверды и тугоплавки, соединения с водородом – летучие вещества, воспламеняющиеся на воздухе. В обычных условиях бор (подобно кремнию) весьма инертен и воздействует лишь с фтором; при нагревании окисляется кислородом, серой, галогенами, азотом. В кислотах, не являющихся окислителями, бор не растворяется. Химическая активность аморфного бора выше, чем кристаллического. Al, Ga и In на воздухе покрыты прочной оксидной пленкой и поэтому не изменяются. Таллий же медленно окисляется. Al – довольно активный амфотерный металл. Очищенный от оксидной пленки он легко реагирует с водой; взаимодействует с неметаллами (галогены, кислород, сера, азот, углерод, фосфор), оксидами, кислотами, щелочами, аммиаком. Пассивируется концентрированными HNO3 и H2SO4 на холоду. Ga, In и Tl по химическим свойствам близки к алюминию, хотя щелочи на Tl не действуют. На рисунках 1 и 2 показано взаимодействие p – элементов III группы с простыми веществами и с важнейшими реагентами.
Рис. 1. Схема взаимодействия р–элементов III группы с простыми веществами
Рис. 2. Схема взаимодействия р–элементов III группы с важнейшими реагентами
Ga + 6HNO3(конц.) = Ga(NO3)3 + 3NO2 + 3H2O 2B(аморфный) + 2KOH + 2H2O = 2KBO2 + 3H2 3Te + 4HNO3(разб.) = 3TeNO3 + NO + 2H2O
1.3. Бинарные соединения
В бинарных соединениях степени окисления для бора +3 и –3, для Al, Ga, In +3, для Tl +1 и +3. Многие бинарные соединения бора похожи по свойствам на аналогичные соединения кремния.
|

 H3BO3
H3BO3  B2O3
B2O3  B (аморфный)
B (аморфный)