Молекулярно-кинетические свойства дисперсных систем
Молекулярно-кинетические свойства дисперсных систем связаны с хаотическим движением частиц дисперсной фазы. К ним относятся: броуновское движение, диффузия, осмотическое давление, седиментация. В качестве характеристики беспорядочного движения частиц был принят средний сдвиг частицы Хаотическое движение частицы охватывает определенный объем пространства, возрастающий во времени. В горизонтальной проекции это соответствует возрастающей площади, пропорциональной квадрату среднего сдвига
где η – вязкость среды, Па∙с. Выражение для коэффициента диффузии:
Диффузия в коллоидных системах протекает несравненно медленнее по сравнению с истинными растворами, так как велики размеры частиц. В коллоидных растворах коэффициент диффузии связан со средним сдвигом:
Седиментация – это свободное оседание частиц в вязкой среде под действием гравитации. Седиментируют достаточно крупные частицы размером более 10-6м. Если частицы имеют сферическую форму, то на основании баланса силы сопротивления вязкой среды (закон Стокса), силы тяжести и выталкивающей силы можно получить формулу для скорости оседания частиц:
где ρ; и ρж – плотность частиц дисперсной фазы и среды соответственно, кг/м3. Следует учитывать то обстоятельство, что эта формула справедлива только при определенных условиях, в которых выполняется закон Стокса. Если известна скорость оседания частиц, то на основании этой формулы можно найти их радиус. При решении задач этого типа может пригодиться и то обстоятельство, что при выполнении закона Стокса частицы оседают с постоянной скоростью, поэтому она может быть вычислена как отношение глубины оседания ко времени оседания:
Осмотическое давление разбавленных дисперсных систем можно вычислить по формуле Вант-Гоффа для истинных растворов, однако вместо молярной концентрации следует подставлять частичную молярную концентрацию, рассчитываемую следующим образом:
Итак, формула Вант-Гоффа для осмотического давления преобразуется к виду:
Осмос для дисперсных систем выражен незначительно, так как частицы слишком массивны.
|

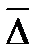 за время t. Это длина отрезка прямой, который соединяет начальную точку движения частицы с ее положением в конечный момент времени, в плоскости горизонтальной проекции, наблюдаемой в микроскоп.
за время t. Это длина отрезка прямой, который соединяет начальную точку движения частицы с ее положением в конечный момент времени, в плоскости горизонтальной проекции, наблюдаемой в микроскоп.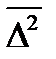 . Эта усредненная величина может быть вычислена на основании статистических законов. В соответствии с теорией Эйнштейна для сферической частицы радиуса r:
. Эта усредненная величина может быть вычислена на основании статистических законов. В соответствии с теорией Эйнштейна для сферической частицы радиуса r: , (2.7.15)
, (2.7.15)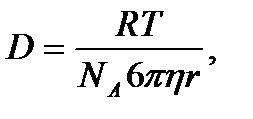 (2.7.16)
(2.7.16) .
. . (2.7.17)
. (2.7.17)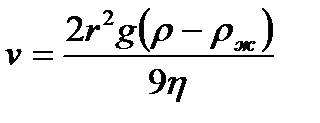 , (2.7.18)
, (2.7.18)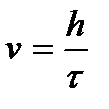 (2.7.19)
(2.7.19)
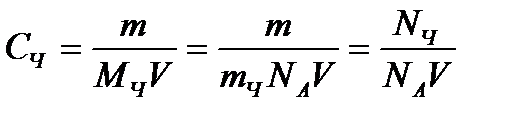 ,
,  (2.7.20)
(2.7.20)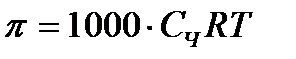 (2.7.21)
(2.7.21)


