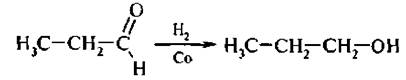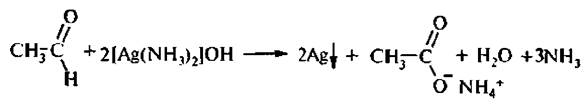Реакции восстановления и окисления
1. Реакции восстановления. Реакцию восстановления альдегидов и кетонов широко используют для получения спиртов. Карбонильные соединения восстанавливаются как при каталитическом гидрировании, так при действии таких восстановителей, как алюмогидрид лития LiAIH4. Альдегиды восстанавливаются до первичных спиртов:
Кетоны восстанавливаются до вторичных спиртов:
2. Реакции окисления. Атьдегнды и кетоны по-разному относятся к действию окислителей. Альдегиды очень легко окисляются, даже при действии слабых окислителей (ионы Ag+, Cu2+). 2.1. Реакция «серебряного зеркала». При действии аммиачного раствора нитрата серебра (реактив Толлеса) на альдегид происходит окислительно-восстановительная реакция. Альдегид окисляется в соответствующую кислоту, а катион серебра восстанавливается в металлическое серебро, которое дает блестящий налет на стенках пробирки.
Эта реакция является качественной для обнаружения альдегидной группы. 2.2. Реакции взаимодействия альдегидов с медно-виннокислъш комплексом. Альдегиды также восстанавливаются реактивом Фелинга (смесь раствора сульфата меди со щелочным раствором натрийкалиевой соли виннокаменной кислоты):
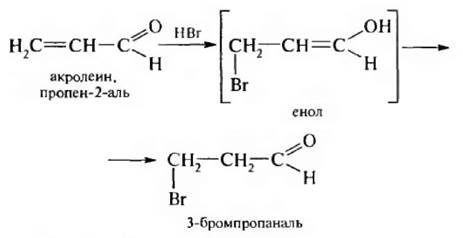
Кетоны к действию этих окислителей инертны. Не окисляются они и кислородом воздуха. Только при действии более сильных окислителей кетоны удается окислить. При этом происходит разрыв углерод-углеродной связи между атомом углерода карбонильной группы и углеводородного радикала и образуется смесь кислот. Альдегиды, содержащие в своей структуре сопряженную систему, имеют ряд особенностей, отличающих их от остальных альдегидов. Присоединение галогеноводородов и воды протекает против правила Марковникова.
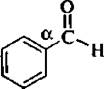
Непредельные альдегиды используются в синтезе ряда соединений, в том числе и лекарственных препаратов. Однако ароматические альдегиды проявляют ряд специфических свойств: 1. Ароматические альдегиды неспособны вступать в альдольную конденсацию. Как вы помните, для того чтобы осуществилась эта реакция, необходимо наличие подвижного атома водорода при а-углерод-ном атоме. В ароматическом альдегиде такого атома водорода нет.
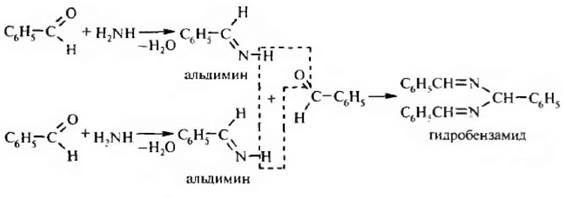
2. Взаимодействие с аммиаком. Реакция ароматических альдегидов с аммиаком – одна из отличительных реакций альдегидов этого ряда.
В этой реакции три молекулы бензальдегида взаимодействуют с двумя молекулами аммиака. Реакция протекает через стадию образования альдимина, который вступает в реакциюс альдегидом с образованием гидробензамида. 3. Реакция Канниццаро – Тищенко. В присутствии сильных оснований или концентрированных щелочей ароматические альдегиды вступают в реакцию диспропорционирования (самоокисления-самовосстановления).
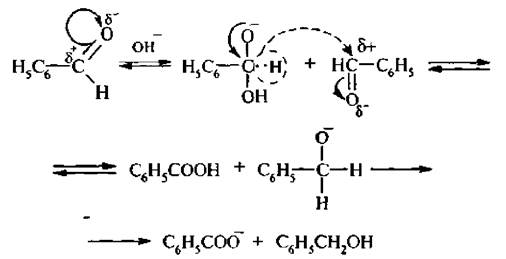
Механизм реакции:
Реакция протекаете переносом гидрид-иона (Н–). Одна молекула альдегида восстанавливается, а другая окисляется и образуются ароматический спирт и кислота. 4. Действие галогена на альдегид. Реакция галогенироватя. В отличие от альдегидов жирного ряда, которые образуют в этих условиях о> галогенсодержашие атьлегиды, ароматические альдегиды образуют гаюгенангидриды ароматических кислот.
5. Бензоиновая конденсация. Альдегиды, которые содержат альдегидную группу в бензольном ядре, способны под действием солей циановодородной кислоты вступать в реакцию бензоиновой конденсации с образованием бензоина.
|