Энергияның шашырауының өлшемі – бұл энтропия
Энтропия деп – жүйедегі ретсіздік өлшемін айтады. Егер жүйеде толық тәртіп орнаса, онда энтропия минимум болады. Ретсіздік артқан сайын энтропия да өседі, егер жүйеде толық ретсіздік яғни ХаОС орнаса, онда энтропия ең жоғарғы мәнге - максимумға ие болады. Қатты дене, сұйық және газдың атомдарының қозғалысын қарастырсақ, онда сұйық атомдарының қатты дене атомдарына қарағанда ретсіз, жүйесіз қозғалыста болатындықтан, сұйықтағы энтропия қатты денеге қарағанда, ал газ атомдарының энтропиясы сұйыққа қарағанда көп болады. Sгаз > Sсұйық > Sқатты дене
Мұндағы Q – жұмысшы дененің тоңазытқышқа берген жылуы, сондықтан да ол теріс. Олай болса
Мұндағы Кез - келген қайтымсыз процесс үшін жылудың келтірілген мөлшерінің қосындысы нольге тең болады, яғни
Бұл Клаузиус теңдеуі деп аталады. Жүйе белгілі бір макро күйге түсу үшін бірнеше микро күйден өтеді. Жүйені макро күйге түсіру үшін қанша микро күйден өткенін көрсететін санды жүйе күйінің термодинамикалық ықтималдылығы деп атайды. Энтропия мен термодинамикалық ықтималдылығы арасындағы байланыс Больцман теңдеуімен анықталады.
S=kℓnW (6) Мұндағы К – Больцман тұрақтысы, W – жүйе күйінің термодинамикалық ықтималдылығы.
Сонымен қайтымды процес үшін S2 -S1 = 0 (8) Қайтымсыз процессте жылу энергиясының шығыны көп болады. S2 - S1 > 0 (9) Тірі жүйеде жұмыс көзінің энергиясы ретінде – химиялық энергия жатады, ол жұмыс пен жылуға айнала алады. Жылу бөлініп азайуы – оның қайтымсыз процесс екенін көрсетеді. Термодинамиканың 2-ші заңының математикалық түрдегі өрнегі.
Тірі жүйеде энтропия ылғида өседі. Энтропия қайтымсыз процессте градиенттің азайу себебінен өседі. Бос энергия Термодинамиканың 2-ші заңы жылу энергиясының жұмысқа айналуын шектейді. Бұл жағдай механикалық, электірлік, химиялық энергияларға да орындалады, себебі осы энергиялардың бір-біріне түрленуі (айналуы) қайтымсыз процесс. Жылу энергиясына қарағанда, бұл энергиялар жоғарғы түрдегі энергияларға жатады, өйткені энергияның бұл түрлері теориялық түрде толығымен п.ә.к. 100% тең жұмысқа айнала алады. Ал жылу энергиясының жұмысқа толығымен айналуын Карно циклі – шектейді. Энергиялардың бұлай бөлінуі – мынаған байланысты: Жылу энергиясы системаны құрайтын микробөлшектердің хаосты түрдегі жылулық қозғалысымен, ал механикалық, электрлік және химиялық энергиялар бөлшектердің реттелген қозғалысымен байланысты және олар өз бетінше жұмысқа айнала алады, ал жылулық энергияның – энергияның басқа түрлеріне ауысуы сырттан қосымша энергия шығынын қажет етеді. Барлық тірі организмдерде негізгі энергияның түрлеріне химиялық – электрлік – механикалық энергиялар жатады, бірақ ол процестердің барлығының да п.ә.к. 100%-тен аспайды. Бұл биологиялық процестердің қайтымсыздығымен түсіндіріледі. Мысалы: Әртүрлі биологиялық процестердің п.ә.к. 1. гликолиз –36% 2. фосфорлық тотығу - 55% 3. бактериялардың жарқырауы 90% дейін 4. бұлшық еттің жиырылуы 30% 5. фотосинтез - 75% Сондықтан да энергияның қанша бөлігі толығымен жұмысқа айнала алатындығын табу керек. Қайтымсыз процесс неғұрлым көп болса, соғұрлым энергия көп болады яғни жұмысқа аинала алатын бөлігі аз болады. Термодинамиканың негізгі теңдеуін жазайық:
TdS = du + dA → du = TdS – dA; – dA = du –TdS; – dA = d (U - TS) (11)
Изотермиялық процесс үшін Т= const пайдалы жұмыс. dA = - d (U - TS) (12) dF = dU – TdS (13) Мұндағы F = U - TS (14) - Термодинамикалық системаның еркін энергиясы деп аталады. Сонда 12-ші теңдеуді былай жаза аламыз dA = - dF (15) Еркін энергияның өзгерісі қайтымды изотермиялық процесс кезіндегі системаның жасаған жұмысына тең болады. Еркін энергия күй функциясы болып табылады, себебі ол ішкі энергияға температураға және энтропияға байланысты өзгереді. 14 – ші теңдеудегі TS – шамасы байлаулы энергия деп аталады. Яғни G = TS (16) Сонда 14 –ші теңдеуді былай жаза аламыз: F = U – G немесе U = F + G (17) 17-шы теңдеу бойынша ішкі энергия еркін энергия мен байланыс энергияларының қосындысына тең болады. Еркін энергияны термодинамикалық системаның потенциалық энергиясы түрінде қарастыруға болады. Сонымен: Еркін (бос) энергия системасының ішкі энергиясының қайтымды изотермиялық процесстер кезінде сыртқы жұмысқа айналатын үлесі болып табылады. Система тепе-тендік қалыпқа ұмтылғанда TdS – байлаулы энергия артады, бұл кезде еркін (бос) энергия кемиді де система тепе-тендік күйге келгенде нөлге тең болады. Сонымен термодинамикалық тепе-тендік энтропияның максимумы мен еркін бос энергияның минимумымен сипаталады. Термодинамиканың І-ші заңын өлі табиғатқа да, тірі табиғатқа да, қолдануға болады, ал термодинамиканың ІІ заңын тірі табиғатқа қолдануға болмайды. Оның себебі тірі организм жабық жүйе емес ашық жүйеге жатады. Жабық жүйеде өзінен-өзі жүретін процестер энтропияның өлуіне ∆S>O1 бос энергияның азаюына әкеліп соқтыратын болса, ашық жүйеде, яғни тірі организмде тепе-теңдік емес процестер – градиенттер пайда болады. Бұл градиенттер тепе-теңдікке келсе организм өледі. Сондықтан да тірі биологиялық организмдерді оны қоршаған ортадан бөліп қарастыруға болмайды. Биологиялық дене өзін қоршаған ортаға өзіне керексіз заттарды және жылу шығарады. Яғни биологиялық организм ашық термодинамикалық жүйе болып саналады. Ал ашық емес жүйеде тепе-теңдік емес процестер жүреді. Бұл процестер стационарлық күйде өтеді, себебі стационарлық күй ашық жүйеге тән болады. Жүйе стационарлық күйге ие болу үшін ол жүйеге сырттан зат және энергия келіп түсіп, содан кейін жүйеден сыртқа зат пен энергия шығып отыруы керек. Олай болса, биологиялық организм стационар күйде болады. өйткені, биологиялық организм өзін қоршаған ортадан зат пен энергия алып, оларды қоршаған ортаға шығарып отырады. Стационар күйде қайтымсыз процестер жүреді; бұл энтропияның өсуіне әкеліп соғады, осыған қарамастан биологиялық организмнің жалпы энтропиясы өзгеріссіз қалады. Сонымен биологиялық жүйенің энтропиясының өзгеруі (∆S) мына теңдікпен аяқталады. ∆S=∆Si+∆Sе (18) Мұндағы: ∆Si- жүйедегі қайтымсыз процестердің әсерінен энтропияның өзгеруі ∆Sе- биологиялық жүйенің өзін қоршаған ортамен әсерлесуі нәтижесінде энтропияның өзгеруі. Процестердің қайтымсыздығы энтропияның өлуіне (∆Si>0), ал күйдің стационарлығы энтропияның өзгеріссіз қалуына әкеліп соқтырады, яғни ∆Se=∆S-Si<0 (19) Бұл теңдік биологиялық жүйеге келіп түсетін заттар энтропиясының (∆Sе) жүйеден шығып кететін заттардың энтропиясынан (∆Si) кем екенін көрсетеді. Сонымен биологиялық жүйе үшін энтропия өзі (S=const) тұрақты болғанымен, оның ортадан алатын энтропиясының өзгеруі ∆Se<01 , ал жүйенің ортаға шығарып жіберетін затының энтропиясының өзгеруі ∆Se>0 болады. Сонымен биологиялық организм мен қоршаған ортаның өскенімен, жалпы организмнің энтропиясы тұрақты болып қалады. 18-ші теңдеді түрлендірсек
Бұл 20-ші теңдеу Пригожин теңдеуі деп аталады. Бұл өрнек организм мен сыртқы ортаның энтропия алмасуының теңдігін көрсетеді. Стацинар күй үшін S=const, Онда Пригожин теңдеуінен стационар күй үшін энтропия өзгерісі нөлге тең болмайды. Бұдан стационар күйде заттар алмасуының үздіксіз болып тұратыны көрінеді. Ашық жүйелердің стационар күйін тұрақты және тұрақты емес деп бөлуге болады. Сыртқы ортаның өзгеруіне байланысты организм стационарлық күйде тұра алатын болса, онда организм осы ортаға үйренеді де өмір сүре береді (адаптацияланады). Ал қоршаған ортаның өзгеруіне байланысты организм стационар күйден ауытқып кететін болса, онда организм өмір сүруін тоқтатады.
|

 (2) осыдан
(2) осыдан 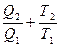 немесе
немесе  (3)
(3) (4)
(4) - жылудың келтірілген мөлшері.
- жылудың келтірілген мөлшері. (5)
(5) мұндағы
мұндағы 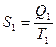
 (7)
(7)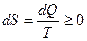 (10)
(10)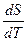 =
= 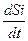 +
+  (20)
(20) =0
=0


