Состояние атома, в котором он потерял все валентные электроны, называется высшей степенью окисления.
Атом, находящийся в высшей степени окисления, может быть только окислителем. В молекуле SO2 и элементарной сере S атом серы находится в промежуточных степенях окисления, т.е., имея валентные электроны, атом может их отдавать, но, не имея завершенного р- подуровня, может и принимать электроны до его завершения. Атом элемента, имеющий промежуточную степень окисления, может проявлять как окислительные, так и восстановительные свойства, что определяется его ролью в конкретной реакции. Так, например роль сульфит-аниона SO 5Na2SO3 +2KMnO4 +3H2SO4 H2SO3 + 2H2S В реакции (7.1) сульфит-анион SO Таким образом, восстановителями могут быть: 1. Простые вещества, атомы которых обладают низкими значениями энергии ионизации и электроотрицательности (в частности, металлы). 2. Сложные вещества, содержащие атомы в низших степенях окисления: H 4. Сложные вещества, содержащие атомы в промежуточных степенях окисления: Na2 Окислителями могут быть: 1. Простые вещества, атомы которых обладают высокими значениями сродства к электрону и электроотрицательности − неметаллы. 2. Сложные вещества, содержащие атомы в высших степенях окисления: K 3. Сложные вещества, содержащие атомы в промежуточных степенях окисления: Na2
|

 в следующих реакциях различна:
в следующих реакциях различна: 2MnSO4 +5Na2SO4 +K2SO4 +3H2O; (7.1)
2MnSO4 +5Na2SO4 +K2SO4 +3H2O; (7.1) в присутствии сильного окислителя KMnO4 играет роль восстановителя; в реакции (7.2) сульфит-анион SO
в присутствии сильного окислителя KMnO4 играет роль восстановителя; в реакции (7.2) сульфит-анион SO  , H2
, H2  ,
,  H3.
H3.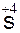 O3,
O3,  Cl2,
Cl2,  (NO3)2.
(NO3)2. O4, K2
O4, K2  2O7, H
2O7, H  O4.
O4. O2,
O2,  SO4.
SO4.


