Вопрос 1. Альдегиды. Их строение, свойства, получение и применение
Ответ. Альдегиды – органические вещества, молекулы которых содержат карбонильную группу С = О, связанную с водородом и углеводородным радикалом.
Общая формула альдегидов: O R - C H Номенклатура Наименование альдегидов производят от исторических названий карбоновых кислот с тем же числом атомов углерода. Так, CH3CHO – уксусный альдегид. По систематической номенклатуре название альдегидов производят от названий углеводородов с прибавлением окончания – аль, CH3CHO – этаналь. Нумерацию углеродной цепи начинают с карбонильной группы. Для разветвленных изомеров перед названием альдегида записывают названия заместителей с указанием цифрой и номера углеродного атома, с которым они связаны: 4 3 2 1 CH3 – CH (CH3) – CH2 – CHO. 3-метилбутаналь
Изомерия Углеродного скелета: CH3 – CH2 – CH2 – CHO – бутаналь, CH3 – CH(CH3) – CHO – 2-метилпропаналь. Классов соединений: CH3 – CH2 – CHO – пропаналь, CH3 – CO – CH3 – пропанон (ацетон). Физические свойства Метаналь – газ, альдегид от C2 до С13 – жидкости, высшее альдегиды – твердые вещества (тетрадеканаль или миристиновый альдегид CH3(CH2)12 CHO имеет температуру плавления 23, 5 Химические свойства 1. Реакции присоединения: а) гидрирование: CH2O + H2 = CH3OH; б) образование ацеталий со спиртами: CH3 - CH2 – CHO + 2C2H5OH = CH3 – CH2 – CH(OC2H5)2 + H2O.
2. Реакция окисления: а) реакция «серебряного зеркала»: CH3CHO + Ag2O
б) взаимодействие с гидрооксидом меди (II): CH3CHO + 2Cu(OH)2 3. Реакции замещения: CH3CH2CHO + Br2 = CH3 – CH (Br) – CHO+ HBr
4.Полимеризация: CH3=O триоксиметилен 5.Поликонденсация: n C6H5OH + n CH2O + n C6H5OH + …= =[ C6H4(OH) – CH2 – C6H4(OH)]n + n H2O Фенолформальдегидная смола Получение а) Окисление
CH4 + O2 метаналь
б) Окисление спиртов: 2CH3OH + O2 в) Реакция Кучерова: C2H2+ H2O г) Окисление алкенов: C2H4 + [O]
Применение: 1. Получение фенолформальдегидных смол, пластмасс. 2. Производство лекарств, формалина (из CH2=O). 3. Производство красителей. 4. Производство уксусной кислоты. 5. Дезинфекция и протравливание семян. Вопрос 2. Проблема защита окружающей среды. Ответ: На сегодняшний день самым крупномасштабным является загрязнение окружающей среды химическими веществами. Охрана атмосферы Источники загрязнения: предприятия чёрной и цветной металлургии, теплоэлектростанции, автотранспорт. Промышленность: выбросы оксидов серы и азота. В результате обжига сульфидных руд цветных металлов выделяется оксид серы (IV). Теплоэлектростанции выделяют SO2 и SO3, которые соединяются с влагой воздуха (SO3 + H2O = H2SO4)и выпадают с виде кислотных дождей. Последствия: из-за переноса воздушных масс в результате выпадения кислотных дождей гибель живого на обширных территориях, а также коррозия металлов, разрушение памятников природы. Теплоэлектростанция и промышленность: сжигание ископаемого топлива приводит к повышению концентрации углекислого газа, нарушению круговорота углерода, парниковому эффекту, а значит, затопление части суши. Автотранспорт загрязняет воздух газами - CO, NxOy, SO2, CxHy, соединениями свинца. Угарный газ в 200 раз активнее кислорода, вызывает поражение гемоглобина; выхлопные газы приводят к смогу. NO + 1/202 = NO2 NO2 O+ O2 = O3. Озон O3 взаимодействует с Cx Hy образуется очень токсичное соединения, то есть смог (туман). Свинец влияет на нервную и ферментативную системы, нарушает обмен веществ; кумулятивный загрязнитель. Ртуть – очень опасна, одинаково эффективно загрязняет все среды обитания. Токсичные соединения металлов попадают в атмосферу с выбросами цветно и чёрной металлургии, а также в результате сжигания мусора и отходов. Охрана гидросферы Источники загрязнения- промышленные и бытовые сточные воды, сельское хозяйство, молевой сплав древесины. Сельское хозяйство: опасность составляют удобрения как минеральные (фосфорные, калийные, нитраты), так и органические. Чрезмерное внесение удобрений приводит к эвтрофикации, она в свою очередь – к «цветению воды» и замору рыбы. Сточные воды: органические отходы, токсичные соединения металлов, волокна (текстиль) - повреждают жабры рыб. Древесина – источник фенолов. Пути решения проблемы загрязнения. 1.Каталитическое разложение NxOy, восстановление метаном или аммиаком. 2.Использовние иных видов топлива. 3.Развитие технологий, получение энергии экологически безопасными способами (солнце, приливы и отливы). 4.Очистка промышленных сточных вод предполагает предварительную фильтрацию, осаждение соединений металлов. Затем предстоит обеззараживание хлором, озоном и биологическая очистка с помощью бактерий. Водоросли, простейшие микроорганизмы биологически очищают воду. После чего её можно сбрасывать в естественные водоёмы. Для очистки воды от солей используется дистилляция, вымораживание (кристаллизация солей). Наиболее эффективный способ - создание экономически рациональных замкнутых систем, обеспечивающих многократное использование вод в производстве. 5.Безотходная технология: сырье – производство – потребление – отходы – вторичное сырье.
|

 ). Низшие альдегиды хорошо растворимы в воде; чем больше атомов углерода в молекуле, тем меньше растворимость; у альдегидов нет водородной связей.
). Низшие альдегиды хорошо растворимы в воде; чем больше атомов углерода в молекуле, тем меньше растворимость; у альдегидов нет водородной связей. 2 Ag + CH3COOH;
2 Ag + CH3COOH; CH3COOH + Cu2O↓ + 2H2O
CH3COOH + Cu2O↓ + 2H2O (CH2O)3.
(CH2O)3. алканов:
алканов: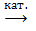 CH2O + H2O.
CH2O + H2O. 2CH2O + 2H2O.
2CH2O + 2H2O. CH3CHO.
CH3CHO. NO + O (hv –УФ-облучение),
NO + O (hv –УФ-облучение),


