Уравнение состояния идеального газа
В процессе разработки молекулярно-кинетичской теории газов для понимания общих законов была выдвинута идея существования гипотетического газа, который строго подчиняется газовым законам при любых температурах и давлении. Этот газ назвали идеальным газом. В идеальном газе молекулы рассматриваются как материальные точки, размеры которых бесконечно малы по сравнению с расстоянием между ними. Кроме того, считается, что столкновение молекул идеально упруги, то есть кроме передачи кинетической энергии никаких других взаимодействий между молекулами идеального газа не существует. Для одного моля идеального газа
Постоянная R называется универсальной газовой постоянной и её значение при нормальных условиях (Р=1, 013·105 Па, Т=273К, V0=22, 4 л) равно
или R=8, 314 Дж/(моль∙ К). Для n молей идеального газа справедливо выражение
Поскольку n=m/M, где m – это масса газа, а M – его молекулярная масса, то PV = Уравнение (61) известно как уравнение Менделеева – Клапейрона, оно связывает все параметры, влияющие на состояние газа. В подавляющем большинстве случаев принимается, что в газообразном состоянии все вещества ведут себя как идеальный газ при давлениях, близких к атмосферному (101, 3 кПа) и ниже.
|

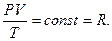 (60)
(60)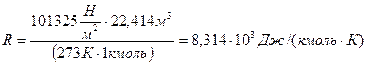
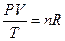 или PV = nRT.
или PV = nRT.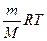 . (61)
. (61)


