Энтропия. Второе начало термодинамики
Понятие энтропии введено в 1865 году Клаузиусом. Для выяснения физического содержания этого понятия рассматривают отношение теплоты Приведенное количество теплоты, сообщаемое телом на бесконечно малом участке процесса равно
Т.е. энтропия замкнутой системы может либо возрастать, либо оставаться постоянной. Энтропия обладает свойством аддитивности: энтропия системы равна сумме энтропий тел, входящих в систему. Вероятностный смысл. Рассмотрим некоторый объем газа в сосуде. Наиболее вероятностное состояние, когда 1/3 молекулы движется по оси Как оценить отклонение системы от этого состояния? Такой характеристикой является энтропия (вероятность состояния). Энтропия – мера неупорядоченности системы. Используя понятие энтропии и неравенство Клаузиуса, второе начало термодинамики можно сформулировать как закон возрастания энтропии замкнутой системы при необратимых процессах: любой необратимый процесс в замкнутой системе происходит так, что энтропия системы возрастает. Или: В процессах, происходящих в замкнутой системе, энтропия не убывает. Или: Невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого к более нагретому. [10, с. 689]
|

 , получающей телом в изотермическом процессе к температуре
, получающей телом в изотермическом процессе к температуре 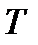 теплоотдающего тела, называемое приведенным количеством теплоты.
теплоотдающего тела, называемое приведенным количеством теплоты. .
. – функция состояния, дифференциалом которой является
– функция состояния, дифференциалом которой является  (приведенное количество теплоты) называется энтропией.
(приведенное количество теплоты) называется энтропией. - неравенство Клаузиуса (при строгом равенстве для обратимых процессов, и при знаке «больше» - для необратимых).
- неравенство Клаузиуса (при строгом равенстве для обратимых процессов, и при знаке «больше» - для необратимых). , 1/3 – по
, 1/3 – по  , 1/3 – по
, 1/3 – по  . Равномерное распределение молекул по всему объему.
. Равномерное распределение молекул по всему объему.


