Теоретическое введение. Количество теплоты, необходимое для нагревания тела массой m от температуры до температуры определяется по формуле
Количество теплоты, необходимое для нагревания тела массой m от температуры Удельной теплоемкостью вещества «с» называется величина равная количеству теплоты, необходимому для нагревания единицы массы вещества на один Кельвин
Молярной теплоемкостью «С» называется физическая величина численно равная количеству теплоты, необходимого для нагревания одного моля вещества на один Кельвин
Молярная и удельная теплоемкости связаны между собой следующим соотношением
где М – молярная масса вещества. Для газов различают две теплоемкости: - - Молярные теплоемкости газа связаны между собой уравнением Майера
где R – универсальная газовая постоянная, численно равная работе, совершаемой одним молем газа при нагревании на один Кельвин при постоянном давлении. Как видно из уравнения /3/ Числом степеней свободы молекулы i называется величина равная числу независимых координат полностью определяющих положение молекулы в пространстве. У одноатомной молекулы i = 3, двухатомной – i =5, трехатомной - i = 6. Молярные теплоемкости газа могут быть выражены через число степеней свободы
И тогда отношение
Одним из методов определения адиабатической постоянной является метод адиабатного расширения газа. Экспериментальная установка представляет собой стеклянный баллон, соединенный с насосом и манометром. С помощью крана баллон может быть соединен с атмосферой (рис. 12.1). Если с помощью насоса накачать в баллон некоторое количество воздуха, то температура и давление внутри него станут выше, чем в окружающей среде. Вследствие теплообмена между воздухом в баллоне и окружающей средой температура в баллоне сравняется с комнатной. Давление воздуха, установившееся в баллоне будет равно
Если теперь на короткий промежуток времени открыть кран, то воздух будет расширяться. Поскольку процесс протекает очень быстро, то его, в первом приближении, можно считать адиабатическим. Давление в баллоне станет равно атмосферному Охладившийся после расширения воздух через некоторое время, вследствие теплообмена, нагреется до температуры окружающей среды
где Переход АВ является адиабатическим и для него справедливо уравнение Пуассона
Переход АС является изотермическим расширением и по закону Бойля-Мариотта
Возведя /10/ в степень
и приравнивая правые части выражений /9/ и /11/ получим
Прологарифмировав выражение /12/ и подставив в него значения давлений
Отсюда
Так как
Выполнение работы. 1. Воздух в баллон накачивают до тех пор, пока разность уровней воды в манометре не достигнет 150 – 200 мм. Когда давление в баллоне установится, записывают значение 2. Открывают кран, и как только из баллона выйдет, накачанный в него воздух, кран быстро закрывают. Значение 3. По формуле /15/ находят значение 4. По формуле /6/ найти теоретическое значение адиабатической постоянной для воздуха 5. Вычислить погрешность измерения.
Контрольные вопросы. 1. Что называется удельной теплоемкостью? Молярной теплоемкостью? 2. Запишите уравнение Майера. 3. Каков физический смысл универсальной газовой постоянной? 4. Что называется числом степеней свободы молекулы? 5. Как молярные теплоемкости выражаются через число степеней свободы? 6. Какой процесс называется адиабатическим? Запишите уравнение Пуассона. 7. Приведите вывод рабочей формулы.
|

 до температуры
до температуры  определяется по формуле
определяется по формуле  , где «с» – удельная теплоемкость вещества.
, где «с» – удельная теплоемкость вещества. . /1/
. /1/ . /2/
. /2/ , /3/
, /3/ - молярная теплоемкость при постоянном объеме;
- молярная теплоемкость при постоянном объеме; - молярная теплоемкость при постоянном давлении.
- молярная теплоемкость при постоянном давлении. , /4/
, /4/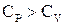 и отношение
и отношение  . Адиабатическая постоянная
. Адиабатическая постоянная  имеет важное значение в термодинамике и ее опытное определение должно быть по возможности более точным.
имеет важное значение в термодинамике и ее опытное определение должно быть по возможности более точным. :
: /5/
/5/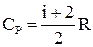 /6/
/6/ /7/
/7/ , /8/
, /8/ где
где 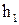 - разность уровней жидкости в манометре. Таким образом первое состояние воздуха в баллоне будет характеризоваться параметрами
- разность уровней жидкости в манометре. Таким образом первое состояние воздуха в баллоне будет характеризоваться параметрами  , точка А на pV – диаграмме (рис. 12.2).
, точка А на pV – диаграмме (рис. 12.2). , а температура
, а температура  (при расширении газ охлаждается). Состояние газа будет характеризоваться параметрами
(при расширении газ охлаждается). Состояние газа будет характеризоваться параметрами  - точка В на pV – диаграмме (рис. 12.2).
- точка В на pV – диаграмме (рис. 12.2). , /8/
, /8/ - разность уровней жидкости в манометре, а состояние газа будет описываться параметрами
- разность уровней жидкости в манометре, а состояние газа будет описываться параметрами  , точка С на pV – диаграмме (рис. 12.2).
, точка С на pV – диаграмме (рис. 12.2). . /9/
. /9/ . /10/
. /10/ /11/
/11/ . /12/
. /12/ и
и  согласно /7/ и /8/ получим
согласно /7/ и /8/ получим . /13/
. /13/ . /14/
. /14/ , то согласно приближенной формуле
, то согласно приближенной формуле  и тогда
и тогда . /15/
. /15/ .
. .
.


