Выполнение работы. Определение спирта в водно-спиртовой смеси по методу П
Определение спирта в водно-спиртовой смеси по методу П. Мартена
В мерную колбу вместимостью 200 см3 пипеткой (бюреткой) вносят 15 см3 раствора бихромата калия и пипеткой (цилиндром) 5 см3 серной кислоты (плотность 1, 84 г/см3) так, чтобы вся кислота соединилась с бихроматом. После этого смесь в колбе перемешивают и охлаждают до 20°С (можно под струёй холодной воды). Порядок приливания реактивов менять не следует! В охлаждённую смесь пипеткой вносят 5 см3 испытуемой смеси спирт-вода, закрывают колбу плотной пробкой и оставляют в покое на 25 мин для проведения реакции окисления спирта бихроматом калия. Увеличение времени выдерживания смеси на ход реакции окисления не влияет. После проведения реакции окисления содержимое колбы доводят дистиллированной водой до метки, тщательно перемешивают, отбирают пипеткой 50 см3 полученной смеси в фарфоровую чашку (химический стакан) и титруют при перемешивании стеклянной палочкой раствором соли Мора для определения остатка бихромата калия, не прореагировавшего со спиртом. Окраска титруемого раствора меняется от тёмного жёлто-зелёного до зелёно-голубоватого цвета к концу титрования. При этом раствор соли Мора приливают по 1-2 капли и степень оттитрованности раствора определяют по изменению окраски выносной капли при слиянии её с каплей индикатора (раствор красной кровяной соли), для чего капли помещают на белую керамическую пластинку. Титрование считается законченным, если капля раствора окрашивается в ярко-голубой цвет при добавлении капли индикатора. Для определения соотношения растворов соли Мора и бихромата калия готовят пробу из бихромата калия и серной кислоты и проводят её титрование. Объём раствора бихромата калия и соли Мора, пошедшего на титрование, характеризует соотношение растворов, которое определяют ежедневно. Обработка результатов Объёмную долю спирта S% определяют по формуле
где: V1 – объём раствора соли Мора, израсходованного на титрование при установлении их соотношения, см3, V4 - объём раствора соли Мора, израсходованного на титрование испытуемой смеси, см3; 15 - объём раствора бихромата калия, взятого для анализа, см3; 0, 0126 – объём безводного спирта, окисляемого 1 см3 раствора бихромата калия, см3; 5 – объём испытуемой смеси, взятой для анализа, см3. Вычисления проводят до второго десятичного знака. За окончательный результат принимают среднеарифметическое значение двух параллельных измерений. Результат округляют до первого десятичного знака. Межлабораторное расхождение результатов составляет не более 0, 1%. Предел абсолютной погрешности ±0, 05%.
Содержание этилового спирта в исследуемом растворе в первом приближении (при экспресс-контроле) определяют на основании эквивалента раствора дихромата калия по спирту. Эквивалент 0, 5 М раствора K2Cr2O7 по спирту рассчитывают из реакции окисления спирта: 2 K2Cr2O7 → 3C2H5OH (11) 2 × 294, 22 г → 3 × 46, 01 г 0, 0245 → x г, где x – количество спирта, окисляемое 1 см3 0, 5М раствора K2Cr2O7, г. x = Эквивалент 0, 5 М раствора K2Cr2O7 по спирту рассчитывают из реакции окисления спирта:
2 K2Cr2O7 → 3C2H5OH (11) 2 × 294, 22 г → 3 × 46, 01 г 0, 0245 → x г, где x – количество спирта, окисляемое 1 см3 0, 5М раствора K2Cr2O7, г. x = При точных определениях учитывают результаты Ι Ι этапа анализа. При этом, исходя из объёмов и концентраций растворов, точно рассчитывается количество молей K2Cr2O7, пошедшее на титрование спирта, и определяемоу количество спирта с использованием уравнений реакций (4) и (11). Решите задачу 2.2.5 [31] (ГОСТ 23268.0-91, ГОСТ 26929-94, ГОСТ 26930-86)
Колориметрическим методом определите массовую долю мышьяка (мг/кг) в минеральной воде. Считать, что: 1. Партия минеральной воды состоит из 250 бутылок. 2. Подготовку проб проводят способом мокрой минерализации 3. Получены следующие результаты: - при построении градуировочного графика по оси абсции отложите значения массы мышьяка (мкг), а по оси ординат – значения оптической плотности (табл. 1); - оптическая плотность испытуемого раствора мышьяка равна 2, 3; - оптическая плотность контрольного раствора мышьяка равна 0, 2.
Определение массы мышьяка колориметрическим методом
Последовательно приведите краткую характеристику загрязнителя, сущность используемого метода анализа и схему проведения контрольного эксперимента: 1. Взятие проб. 2. Подготовка проб. 3. Проведение анализа. 4. Обработка результатов. На основании полученных данных сделайте вывод о соответствии исследуемого продукта СанПиН 2.3.2.1078-01 «Гигиенические требования безопасности и пищевой ценности пищевых продуктов». Контрольные вопросы
|

 (6.12)
(6.12)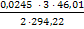 = 0, 00575 (г) или 0, 00575: 0, 789 = 0, 0073 (см3)
= 0, 00575 (г) или 0, 00575: 0, 789 = 0, 0073 (см3)


