В организме человека
| Элемент
| Типичный симптом при дефиците
| | Co
| Замедление роста скелета
| | Mg
| Мышечные судороги
| | Fe
| Анемия, нарушение иммунной системы.
| | Zn
| Повреждение кожи, замедление роста, замедление сексуального созревания
| | Cu
| Слабость артерий, нарушение деятельности печени, вторичная анемия
| | Mn
| Бесплодность, ухудшение роста скелета
| | Mo
| Замедление клеточного роста, склонность к кариесу.
| | Co
| Злокачественная анемия
| | Ni
| Учащение депрессий, дерматиты
| | Cr
| Симптомы диабета
| | Si
| Нарушение роста скелета
| | F
| Кариес зубов
| | I
| Нарушение работы щитовидной железы.
| | Se
| Мускульная (в частности сердечная) слабость
| 3. Константы растворимости некоторых малорастворимых
солей и гидроксидов (25оС)
| Вещество
| Ks
| Вещество
| Ks
| | AgBr
| 5,3×10–13
| FeC2O4
| 2,0×10–7
| | AgCl
| 1,78×10–10
| Fe(OH)2
| 1,0×10–15
| | AgI
| 8,3×10–17
| Fe(OH)3
| 3,2×10–38
| | Ag2CO3
| 1,2×10–12
| FePO4
| 1,3×10–22
| | Ag2C2O4
| 3,5×10–11
| FeS
| 5,0×10–18
| | Ag2CrO4
| 1,1×10–12
| Hg2Cl2
| 1,3×10–18
| | Ag2Cr2O7
| 1,0×10–10
| HgS
| 4,0×10–53
| | AgCN
| 1,4×10–16
| Hg2SO4
| 6,8×10–7
| | AgSCN
| 1,1×10–12
| Li2CO3
| 3,98×10–3
| | AgNO2
| 1,6×10–4
| LiF
| 3,8×10–3
| | Ag3PO4
| 1,3×10–20
| Li3PO4
| 3,2×10–9
| | Ag2S
| 6,3×10–50
| MgCO3
| 4,0×10–5
| | Ag2SO3
| 1,5×10–14
| MgC2O4
| 8,6×10–5
| | Ag2SO4
| 1,6×10–5
| Mg(OH)2
| 6,0×10–10
| | Al(OH)3
| 1,0×10–32
| Mg3(PO4)2
| 1,0×10–13
| | AlPO4
| 5,7×10–19
| MnCO3
| 1,8×10–11
| | AuBr
| 5,0×10–17
| Mn(OH)2
| 4,5×10–13
| | AuCl
| 2,0×10–13
| MnS
| 2,5×10–10
| | Вещество
| Ks
| Вещество
| Ks
| | AuI
| 1,6×10–23
| PbBr2
| 9,1×10–6
| | BaCO3
| 4,0×10–10
| PbCl2
| 1,6×10–5
| | BaC2O4
| 1,1×10–7
| PbI2
| 1,1×10–9
| | BaCrO4
| 1,2×10–10
| PbCO3
| 7,5×10–14
| | BaF2
| 1,1×10–6
| PbC2O4
| 4,8×10–10
| | Ba(OH)2
| 5,0×10–3
| PbCrO4
| 1,8×10–14
| | Ba3(PO4)2
| 6,0×10–39
| Pb(OH)2
| 1,1×10–20
| | BaSO3
| 8,0×10–7
| Pb3(PO4)2
| 7,9×10–43
| | BaSO4
| 1,1×10–10
| PbS
| 2,5×10–27
| | CaCO3
| 3,8×10–9
| PbSO4
| 1,6×10–8
| | CaC2O4
| 2,3×10–9
| Sr(OH)2
| 3,2×10–4
| | CaC4H4O6
| 7,7×10–7
| SrCO3
| 1,1×10–10
| | CaF2
| 4,0×10–11
| SrC2O4
| 1,6×10–7
| | Ca(OH)2
| 5,5×10–6
| Sr3(PO4)2
| 1,0×10–31
| | Ca(H2PO4)2
| 1,0×10–3
| SrSO3
| 4,0×10–8
| | CaHPO4
| 2,7×10–7
| SrSO4
| 3,2×10–7
| | Ca3(PO4)2
| 2,0×10–29
| TlBr
| 3,9×10–6
| | CaSO3
| 3,2×10–7
| TlCl
| 1,7×10–4
| | CaSO4
| 2,5×10–5
| TlI
| 5,75×10–8
| | CdCO3
| 1,0×10–12
| Tl2CO3
| 4,0×10–3
| | CdC2O4
| 1,5×10–8
| Tl2C2O4
| 2,0×10–4
| | CdS
| 1,0×10–29
| Tl3PO4
| 6,7×10–8
| | Cr(OH)3
| 6,3×10–31
| Tl2S
| 5,0×10–21
| | Cu(OH)2
| 5,0×10–20
| Tl2SO3
| 6,3×10–4
| | CuS
| 6,3×10–36
| Tl2SO4
| 4,0×10–3
| | Cu2S
| 2,5×10–48
| Zn(OH)2
| 7,1×10–18
| |
|
| ZnS
| 1,6×10–24
|
4. Константы нестойкости комплексных ионов в водных растворах (25оС)
| M n+
| Лиганд
| Константа
| M n+
| Лиганд
| Константа
| | Al3+
| ОН–
| K 1-4 = 1×10–33
| Cu2+
| Гистидин
| K 1-2=4,68×10–19
| | Zn2+
| ОН–
| K 1-4 = 1,99×10–18
| Zn2+
| Гистидин
| K 1-2=1,32×10–13
| | Cu2+
| ОН–
| K 1-4 = 2,75×10–15
| Al3+
| ЭДТА4–-ион
| K 1 = 3,2×10–17
| | Cr3+
| ОН–
| K 1-4 = 1,26×10–30
| Ba2+
| ЭДТА4–-ион
| K 1 = 1,7×10–8
| | Cd2+
| ОН–
| K 1-4 = 2×10–9
| Bi3+
| ЭДТА4–-ион
| K 1 = 4,0×10–28
| | Zn
| (H2O)
| K 1-4 = 2,1×10–10
| Ca2+
| ЭДТА4–-ион
| K 1 = 2,6×10–11
| | Ag+
| NH3
| K 1-2 = 5,9×10–8
| Cd2+
| ЭДТА4–-ион
| K 1 = 3,5×10–17
| | Cd2+
| NH3
| K 1-4 = 2,8×10–7
| Co2+
| ЭДТА4–-ион
| K 1 = 4,9×10–17
| | Co2+
| NH3
| K 1-4 = 8,5×10–6
| Co3+
| ЭДТА4–-ион
| K 1 = 2,5×10–41
| | Co2+
| NH3
| K 1-6 = 4,1×10–5
| Cr3+
| ЭДТА4–-ион
| K 1 = 4,0×10–21
| | Co3+
| NH3
| K 1-6 = 6,2×10–36
| Cu2+
| ЭДТА4–-ион
| K 1 = 1,6×10–19
| | Cu2+
| NH3
| K 1-4 = 1,1×10–12
| Fe2+
| ЭДТА4–-ион
| K 1 = 6,3×10–15
| | Hg2+
| NH3
| K 1-4 = 5,0×10–20
| Fe3+
| ЭДТА4–-ион
| K 1 = 5,9×10–25
| | Ni2+
| NH3
| K 1-4 = 3,4×10–8
| Hg2+
| ЭДТА4–-ион
| K 1 = 1,6×10–22
| | Zn2+
| NH3
| K 1-4 = 8,3×10–12
| Mg2+
| ЭДТА4–-ион
| K 1 = 7,6×10–10
| | Al3+
| F–
| K 1-6 = 2,1×10–21
| Mn2+
| ЭДТА4––ион
| K 1 = 9,1×10–15
| | Al3+
| F–
| K 1-6 = 2,1×10–21
| Pb2+
| ЭДТА4––ион
| K 1 = 9,1×10–19
| | Fe3+
| F–
| K 1-6 = 7,9×10–17
| Tl+
| ЭДТА4––ион
| K 1 = 2,9×10–7
| | Bi3+
| Br–
| K 1-6 = 3,0×10–10
| Tl3+
| ЭДТА4––ион
| K 1 = 1,6×10–38
| | Hg2+
| Br–
| K 1-4 = 1,0×10–21
| Zn2+
| ЭДТА4––ион
| K 1 = 5,5×10–17
| | Pt2+
| Br–
| K 1-4 = 3,2×10–21
| Ca2+
| Тартрат-ион
| K 1-2 = 9,8×10–10
| | Bi3+
| Cl–
| K 1-6 = 3,8×10–7
| Fe3+
| Тартрат-ион
| K 1-2 = 1,4×10–12
| | Pt2+
| Cl–
| K 1-4 = 1×10–16
| Ca2+
| Цитрат-ион
| K 1 = 2,1×10–5
| | Bi3+
| I–
| K 1-6 = 7,98×10–20
| Mg2+
| Цитрат-ион
| K 1 = 1,1×10–4
| | Hg2+
| I–
| K 1-4 = 1,5×10–30
| Cu2+
| Цитрат-ион
| K 1 = 1,3×10–6
| | Pb2+
| I–
| K 1-4 = 1,2×10–4
| Hg2+
| Цитрат-ион
| K 1 = 1,3×10–11
| | Cd2+
| I–
| K 1-5 = 7,1×10–6
| Mg2+
| Глицинат-ион
| K 1-2 = 3,5×10–7
| | Hg2+
| I–
| K 1-4 = 1,48×10–30
| Ca2+
| Глицинат-ион
| K 1 = 4,2×10–2
| | Ag+
| CN–
| K 1-2 = 1,4×10–20
| Mn2+
| Глицинат-ион
| K 1 = 3,6×10–4
| | Au+
| CN–
| K 1-2 = 5,0×10–30
| Fe2+
| Глицинат-ион
| K 1-2 = 1,6×10–8
| | Cd2+
| CN–
| K 1-4 = 7,8×10–18
| Co2+
| Глицинат-ион
| K 1-2 = 5,6×10–10
| | Co2+
| CN–
| K 1-6 = 8,1×10–20
| Ni2+
| Глицинат-ион
| K 1-2 = 2,7×10–11
| | Co3+
| CN–
| K 1-6 = 1×10–64
| Cu2+
| Глицинат-ион
| K 1-2 = 2,6×10–16
| | Cu+
| CN–
| K 1-4 = 2,0×10–30
| Zn2+
| Глицинат-ион
| K 1-2 = 1,1×10–10
| | Fe2+
| CN–
| K 1-6 = 1,3×10–37
| Mn2+
| Цистеинат-ион
| K 1 = 7,94×10–5
| | Fe3+
| CN–
| K 1-6 = 1,3×10–44
| Fe2+
| Цистеинат-ион
| K 1-2 = 1,7×10–12
| | Ni2+
| CN–
| K 1-4 = 1,0×10–31
| Co2+
| Цистеинат-ион
| K 1-2=1,26×10–17
| | Ag+
| SCN–
| K 1-2 = 5,9×10–9
| Ni2+
| Цистеинат-ион
| K 1-2=5,01×10–20
| | M n+
| Лиганд
| Константа
| M n+
| Лиганд
| Константа
| | Bi3+
| SCN–
| K 1-6 = 5,9×10–5
| Zn2+
| Цистеинат-ион
| K 1-2 = 2,0×10–19
| | Co2+
| SCN–
| K 1-3 = 1,6×10–2
| Mg2+
| Аспаргиновая к-та
| K 1=3,72×10–5
| | Cu2+
| SCN–
| K 1-3 = 3,0×10–7
| Ca2+
| Аспаргиновая к-та
| K 1=2,51×10–2
| | Fe3+
| SCN–
| K 1-6 = 5,9×10–4
| Mn2+
| Аспаргиновая к-та
| K 1=1,82×10–4
| | Hg2+
| SCN–
| K 1-4 = 6,3×10–22
| Co2+
| Аспаргиновая к-та
| K 1-2=6,61×10–11
| | Ag+
| S2O 
| K 1-3 = 7,1×10–15
| Cu2+
| Аспаргиновая к-та
| K 1-2=4,47×10–16
| | Cd2+
| S2O 
| K 1-3 = 6,3×10–9
| Zn2+
| Аспаргиновая к-та
| K 1-2=7,08×10–11
| | Cu+
| S2O 
| K 1-3 = 1,9×10–14
| Mg2+
| Глутаминовая к-та
| K 1=1,26×10–2
| | Pb2+
| S2O 
| K 1-4 = 6,3×10–8
| Ca2+
| Глутаминовая к-та
| K 1 = 8,91×10–3
| | Hg2+
| S2O 
| K 1-4 = 2,4×10–34
| Mn2+
| Глутаминовая к-та
| K 1 = 5,01×10–4
| | Ag+
| SO 
| K 1-3 = 1×10–9
| Fe2+
| Глутаминовая к-та
| K 1 = 2,51×10–5
| | Cu+
| SO 
| K 1-3 = 4,4×10–10
| Co2+
| Глутаминовая к-та
| K 1-2 = 3,47×10–9
| | Hg2+
| SO 
| K 1-3 = 1,1×10–25
| Ni2+
| Глутаминовая к-та
| K 1-2=4,57×10–11
| | Ag+
| NO 
| K 1-2 = 1,5×10–3
| Cu2+
| Глутаминовая к-та
| K 1-2=3,98×10–15
| | Cd2+
| NO 
| K 1-3 = 1,5×10–4
| Zn2+
| Глутаминовая к-та
| K 1-2=3,47×10–10
| | Al3+
| C2O 
| K 1-3 = 5,0×10–17
| Ni2+
| Салицилат-ион
| K 1-2 = 1,8×10–12
| | Cr3+
| C2O 
| K 1-3 = 3,6×10–16
| Cu2+
| Салицилат-ион
| K 1-2 = 2,0×10–21
| | Fe3+
| C2O 
| K 1-3 = 6,3×10–21
| Co3+
| Салицилат-ион
| K 1-2 = 3,8×10–12
| | Mn3+
| C2O 
| K 1-3 = 3,8×10–20
| Fe3+
| Салицилат-ион
| K 1-3 = 5,4×10–37
| | Ca2+
| Серин
| K 1 ~ 0,32
| Mg2+
| Глицил-глицин
| K 1 = 8,7×10–2
| | Fe2+
| Серин
| K 1 = 10–7
| Ca2+
| Глицил-глицин
| K 1 = 5,75×10–2
| | Co2+
| Серин
| K 1 = 10–8
| Mn2+
| Глицил-глицин
| K 1 = 7,08×10–3
| | Cu2+
| Серин
| K 1-2=2,83×10–15
| Co2+
| Глицил-глицин
| K 1-2=1,32×10–6
| | Mg2+
| Пролин
| K > 10–4
| Cu2+
| Глицил-глицин
| K 1-2=2,19×10–12
| | Mn2+
| Пролин
| K 1-2 = 3,16×10–6
| Zn2+
| Глицил-глицин
| K 1-2=2,69×10–7
| | Fe2+
| Пролин
| K 1-2=5,01×10–9
| Mg2+
| Аспаргин
| K 1-2 = 10–4
| | Co2+
| Пролин
| K 1-2=5,01×10–10
| Mn2+
| Аспаргин
| K 1-2 ~ 3,2×10–5
| | Cu2+
| Пролин
| K 1-2=1,58×10–17
| Fe2+
| Аспаргин
| K 1-2=3,16×10–19
| | Zn2+
| Пролин
| K 1-2=6,31×10–11
| Co2+
| Аспаргин
| K 1-2=7,41×10–9
| | Mn2+
| Лизин
| K 1 = 10–2
| Ni2+
| Аспаргин
| K 1-2=2,51×10–11
| | Fe2+
| Лизин
| K 1 = 3,16×10–5
| Cu2+
| Аспаргин
| K 1-2=1,26×10–15
| | Co2+
| Лизин
| K 1-2 = 1,68×10–7
| Zn2+
| Аспаргин
| K 1-2 = 2,0×10–9
| | Ni2+
| Лизин
| K 1-2 = 1,58×10–9
| Mn2+
| Гли-Гли-Гли
| K 1 = 3,89×10–2
| | Cu2+
| Лизин
| K 1-2 = 2,0×10–14
| Co2+
| Гли-Гли-Гли
| K 1-2=2,57×10–6
| | Zn2+
| Лизин
| K 1-2 = 2,51×10–8
| Cu2+
| Гли-Гли-Гли
| K 1-2=2,75×10–11
| | Mn2+
| Гистидин
| K 1-2=1,82×10–8
| Zn2+
| Гли-Гли-Гли
| K 1-2=4,79×10–7
| | Fe2+
| Гистидин
| K 1-2=5,01×10–10
| Ni2+
| Гистидин
| K 1-2=1,26×10–16
| | Co2+
| Гистидин
| K 1-2=1,38×10–14
|
|
|
| | | | | | | | | 5. Стандартные восстановительные (редокс) потенциалы (25оС)
| Полуреакция
| jо, В
| Полуреакция
| jо, В
| | Ag+ + e Ag¯
| +0,80
| [Mn(CN)6]3–+ e [Mn(CN)6]4–
| –0,24
| | [Ag(NH3)2]++ e Ag¯ + 2NH3
| +0,373
| MnO 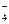 + e MnO + e MnO 
| +0,56
| | AgCl + e Ag¯ + Cl–
| +0,283
| MnO  +8H++5 e Mn2++4H2O +8H++5 e Mn2++4H2O
| +1,51
| | Au+ + e Au¯
| +1,68
| MnO  +2H2O+3 e MnO2+4OH– +2H2O+3 e MnO2+4OH–
| +0,60
| | Au3+ + 2 e Au+
| +1,41
| [Mo(CN)6]3–+ e [Mo(CN)6]4–
| +0,73
| | Au3+ + 3 e Au¯
| +1,50
| N2 + 8H+ + 6 e 2NH 
| +0,26
| | Br2 + 2 e 2Br–
| +1,09
| NO  +H2O+ e NO +H2O+ e NO  +2OH– +2OH–
| +0,01
| | HBrO + H+ + 2 e Br– + H2O
| +1,34
| NO  +3H++2 e HNO2+H2O +3H++2 e HNO2+H2O
| +0,94
| BrO 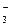 +5H++4 e HBrO+2H2O +5H++4 e HBrO+2H2O
| +1,45
| NO 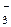 + 2H+ + e NO2 + H2O + 2H+ + e NO2 + H2O
| +0,80
| | Cl2 + 2 e 2Cl–
| +1,36
| NO  +H2O+ e NO2+2OH– +H2O+ e NO2+2OH–
| –0,86
| | Co3+ + e Co2+
| +1,95
| NO  +4H++3 e NO+2H2O +4H++3 e NO+2H2O
| +0,96
| | Co2+ + 2 e Co¯
| –0,29
| NO  +2H2O+3 e NO+4OH– +2H2O+3 e NO+4OH–
| –0,14
| | Co3+ + 3 e Co¯
| +0,46
| HNO2 + H+ + e NО + H2O
| +1,00
| | [Co(NH3)6]3++ e [Co(NH3)6]2+
| +0,1
| O2 + 4H+ +4 e 2H2O
| +1,23
| | Cr3+ + e Cr2+
| –0,41
| O2 + 4H+ +4 e 2H2O (pH=7)
| +0,82
| Cr2O  +14H++6 e 2Cr3++7H2O +14H++6 e 2Cr3++7H2O
| +1,33
| O2 + 2H2O + 4 e 4OH–
| +0,40
| | [Cr(CN)6]3- + e [Cr(CN)6]4–
| –1,28
| O2 + 2H+ + 2 e H2O2
| +0,68
| | Cu+ + e Cu¯
| +0,53
| O2+H2O+2 e HO  +OH– +OH–
| –0,08
| | Cu2+ + 2 e Cu¯
| +0,35
| H2O2 + 2H+ + 2 e 2H2O
| +1,77
| | Cu2+ + e Cu+
| +0,16
| HO  + H2O + 2 e 3OH– + H2O + 2 e 3OH–
| +0,88
| | Cu2+ + I– + e CuI
| +0,86
| O3 + 2H+ + 2 e O2 + H2O
| +2,07
| | F2 + 2 e 2F–
| +2,77
| O3 + H2O + 2 e O2 + 2OH–
| +1,24
| | Fe3+ + e Fe2+
| +0,77
| S + 2H+ + 2 e H2S
| +0,17
| | [Fe(CN)6]3– + e [Fe(CN)6]4–
| +0,36
| S + 2 e S2–
| –0,48
| | 2H+ + 2 e H2
| 0,00
| SO 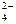 +4H++2 e SO2+2H2O +4H++2 e SO2+2H2O
| +0,17
| | 2H+ + 2 e H2 (pH = 7)
| –0,414
| SO  +H2О+2 e SO +H2О+2 e SO  +2ОН– +2ОН–
| –0,93
| 2Hg2+ + 2 e Hg 
| +0,91
| S4O  + 2 e 2S2O + 2 e 2S2O 
| +0,09
| | Hg2+ + 2 e Hg¯
| +0,85
| Sn2+ + 2 e Sn ¯
| –0,14
| Hg 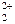 + 2 e 2Hg + 2 e 2Hg
| +0,80
| Sn4+ + 2 e Sn2+
| +0,15
| | I2 +2е 2I–
| +0,54
| Tl+ + e Tl ¯
| –0,36
| IO 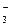 + 5H+ + 4 e HIO+2H2O + 5H+ + 4 e HIO+2H2O
| +1,14
| Tl3+ + 2 e Tl+
| +1,25
| | HIO + H+ + 2 e I– + H2O
| +0,99
| Zn2+ + 2 e Zn¯
| –0,76
| | Mn3+ + e Mn2+
| +1,51
| [Zn(NH3)4]2+ + 2 e Zn¯+4NH3
| –1,04
| | Cd2+ + 2 e Cd¯
| –0,403
|
|
|
Содержание химических элементов в земной коре, почве, морской воде, растениях, животных (по В.И. Вернадскому)
| Элемент
| Массовая доля, %, в
| | земной коре
| почве
| морской воде
| растениях
| животных
| |
|
|
|
|
|
| | O
| 49,4
| 49,0
| 85,82
| 70,0
| 62,4
| | Si
| 27,6
| 33,0
| 5×10–5
| 0,15
| 1×10–5
| | Al
| 7,45
| 7,12
| 1×10–6
| 0,02
| 1×10–5
| | Fe
| 5,0
| 3,8
| 5×10–6
| 0,02
| 0,01
| | C
| 0,15
| 2,0
| 0,002
|
|
| | Ca
| 3,5
| 1,37
| 0,04
| 0,3
| 1,9
| | K
| 2,5
| 1,36
| 0,038
| 0,3
| 0,27
| | Na
| 2,6
| 0,63
| 1,06
| 0,02
| 0,1
| | Mg
| 2,0
| 0,6
| 0,14
| 0,07
| 0,03
| | Ti
| 0,6
| 0,46
| 1×10–7
| 1×10–7
| 1×10–6–1×10–5
| | N
| 0,02
| 0,1
| 1×10–5
| 0,3
| 3,1
| | H
| 1,0
| –
| 10,72
|
| 9,7
| | P
| 0,08
| 0,08
| 5×10–5
| 0,07
| 0,95
| | S
| 0,05
| 0,05
| 0,09
| 0,05
| 0,16
| | Mn
| 0,09
| 0,085
| 4×10–7
| 1×10–3
| 1×10–5
| | Zr
| 0,04
| 0,62
| –
| 5×10–4
| –
| | Sr
| 0,04
| 0,03
| 1×10–3
| 10–1
| 1×10–3
| | Ba
| 0,04
| 0,04
| 5×10–6
| 10–4
| 1×10–5
| | Ge
| 0,02
| 0,02
| 1×10–7
| –
| 1×10–6
| | Cr
| 0,02
| 0,019
| –
| 5×10–4
| 1×10–5
| | F
| 0,027
| 0,02
| 1×10–4
| 1×10–5
| 1×10–5–1×10–4
| | V
| 0,03
| 0,01
| 5×10–8
| 1×10–4
| 1×10–5
| | Cl
| 0,048
| 0,01
| 1,89
| 1×10–2
| 0,08
| | Rb
| 0,03
| 5×10–3
| 2×10–5
| 5×10–4
| 1×10–5
| | Zn
| 5×10–3
| 5×10–3
| 5×10–6
| 3×10–4
| 1×10–3
| | Ni
| 1×10–2
| 5×10–3
| 3×10–7
| 5×10–5
| 1×10–6
| | Cu
| 1×10–2
| 2×10–3
| 2×10–6
| 2×10–4
| 1×10–4
| | Co
| 4×10–3
| 1×10–3
| 1×10–7
| 2×10–5
| 1×10–6–1×10–5
| | Li
| 6,5×10–3
| 3×10–3
| 1,5×10–5
| 1×10–5
| 1×10–4
| | Pb
| 1,5×10–4
| 5×10–4
| 5×10–7
| 1×10–5
| 1×10–6
| | B
| 3×10–4
| 5×10–4
| 5×10–4
| 1×10–4
| 1×10–5
| | I
| 3×10–5
| 5×10–4
| 1×10–6
| 1×10–5
| 1×10–5–1×10–4
| | Mo
| 1,5×10–2
| 3×10–4
| 1×10–7
| 2×10–5
| 1×10–6–1×10–5
| | As
| 5×10–4
| 4×10–4
| 1,5×10–6
| 3×10–5
| 1×10–6–1×10–5
| | Br
| 1,5×10–4
| 2×10–4
| 7×10–3
| –
| 1×10–4
| | Cd
| 5×10–5
| 5×10–6
| –
| 1×10–6
| 1×10–4
| |
|
|
|
|
|
| | Th
| 1×10–3
| 6×10–4
| 4×10–8
| 6×10–4
| 1×10–7
| | W
| –
| 1×10–4
| –
| –
| –
| | U
| 2×10–4
| 1×10–4
| 2×10–7
| –
| 1×10–8
| | Se
| 6×10–5
| 1×10–6
| 4×10–7
| 1×10–7
| –
| | Bi
| 1,7×10–6
| 2×10–8
| 2×10–8
| –
| 2×10–6
| | Hg
| 7×10–6
| 1×10–6
| 3×10–7
| 1×10–7
| 1×10–7–1×10–6
| | Ag
| 1×10–6
| –
| 7×10–9
| –
| 5×10–6–1×10–6
| | Au
| 5×10–7
| –
| 4×10–10
| –
| 1×10–7
| | Ra
| 2×10–10
| 8×10–11
| 1×10–14
| 1×10–14
| 1×10–12
|

Шрифт зодчего Шрифт зодчего состоит из прописных (заглавных), строчных букв и цифр...
|

Картограммы и картодиаграммы Картограммы и картодиаграммы применяются для изображения географической характеристики изучаемых явлений...
|

Практические расчеты на срез и смятие При изучении темы обратите внимание на основные расчетные предпосылки и условности расчета...
|

Функция спроса населения на данный товар Функция спроса населения на данный товар: Qd=7-Р. Функция предложения: Qs= -5+2Р,где...
|
Мотивационная сфера личности, ее структура. Потребности и мотивы. Потребности и мотивы, их роль в организации деятельности...
Классификация ИС по признаку структурированности задач Так как основное назначение ИС – автоматизировать информационные процессы для решения определенных задач, то одна из основных классификаций – это классификация ИС по степени структурированности задач...
Внешняя политика России 1894- 1917 гг. Внешнюю политику Николая II и первый период его царствования определяли, по меньшей мере три важных фактора...
|
Понятие и структура педагогической техники Педагогическая техника представляет собой важнейший инструмент педагогической технологии, поскольку обеспечивает учителю и воспитателю возможность добиться гармонии между содержанием профессиональной деятельности и ее внешним проявлением...
Репродуктивное здоровье, как составляющая часть здоровья человека и общества
Репродуктивное здоровье – это состояние полного физического, умственного и социального благополучия при отсутствии заболеваний репродуктивной системы на всех этапах жизни человека...
Случайной величины Плотностью распределения вероятностей непрерывной случайной величины Х называют функцию f(x) – первую производную от функции распределения F(x):
Понятие плотность распределения вероятностей случайной величины Х для дискретной величины неприменима...
|
|




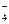 + e MnO
+ e MnO 
 +8H++5 e Mn2++4H2O
+8H++5 e Mn2++4H2O
 +2H2O+3 e MnO2+4OH–
+2H2O+3 e MnO2+4OH–

 +H2O+ e NO
+H2O+ e NO  +2OH–
+2OH–
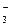 +5H++4 e HBrO+2H2O
+5H++4 e HBrO+2H2O
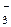 + 2H+ + e NO2 + H2O
+ 2H+ + e NO2 + H2O
 +14H++6 e 2Cr3++7H2O
+14H++6 e 2Cr3++7H2O
 +OH–
+OH–
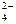 +4H++2 e SO2+2H2O
+4H++2 e SO2+2H2O
 +H2О+2 e SO
+H2О+2 e SO  +2ОН–
+2ОН–

 + 2 e 2S2O
+ 2 e 2S2O 
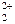 + 2 e 2Hg
+ 2 e 2Hg



