Химическая кинетика равновесие
Химической кинетикой называется учение о скорости и механизмах химических реакций, закономерностях их развития во времени. При постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, возведенных в некоторых степенях:
А+В+2D = F+L
где k −; коэффициент пропорциональности, называемый константой скорости данной реакции. Первая попытка учесть влияние температуры на скорость химических реакций сделана Вант-Гоффом, сформулировавшим следующее эмпирическое правило. При повышении температуры на каждые 10 градусов константа скорости элементарной химической реакции увеличивается в 2 − 4 раза. Величина, показывающая, во сколько раз увеличивается скорость или константа скорости при повышении температуры на 10 градусов, есть температурный коэффициент скорости реакции γ;. Математически правило Вант-Гоффа можно записать следующим образом:
где g − температурный коэффициент скорости химической реакции; k1, k2 – константы скорости реакции при соответствующих температурах; t1, t2 – температуры реакций. Более точно зависимость скорости реакции от температуры описывает уравнение Аррениуса:
где A − стерический фактор, который определяет вероятность активного столкновения; Ea – энергия активации; R – универсальная газовая постоянная; T – температура реакции. Величина Ea характеризует природу реагирующих веществ и определяется экспериментально из зависимости k = f(T). Записав уравнение (3.3) в логарифмическом виде и решая его для констант при двух температурах, находим Ea:
В соответствии с законом действующих масс состояние равновесной химической системы характеризуется константой равновесия, представляющей собой отношение констант скоростей прямой (k1) и обратной (k2) реакций [4].
где а = νа, b = νb, c = νc, d = νd.
|

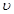 = k∙CA∙CB ∙ CD 2, (3.1)
= k∙CA∙CB ∙ CD 2, (3.1) , (3.2)
, (3.2) , (3.3)
, (3.3) ,
, . (3.4)
. (3.4) , (3.5)
, (3.5)


