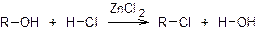Реакция с солянокислым раствором хлорида цинка (Проба Лукаса).
Концентрированные галогенводородные кислоты способны замещать гидроксильную группу в спиртах на галоген, образуя нерастворимые в воде галогенпроизводные. Но замещение происходит с различной скоростью в зависимости от природы спирта. Первичные, вторичные и третичные спирты различаются по реакции их с соляной кислотой в присутствии хлорида цинка и без него. Так, третичные спирты реагируют с конц. соляной кислотой без хлорида цинка при комнатной температуре уже в течение 5 минут, а вторичные и первичные спирты при этом не реагируют. В присутствии хлорида цинка третичные спирты взаимодействуют с соляной кислотой в течение 3-5 минут, при этом получаются нерастворимые в воде капли галоидного алкила. Вторичные спирты сначала растворяются с образованием прозрачного раствора, а затем раствор мутнеет и выпадают капли галогенпроизводного. Реакция для них возможна лишь при длительном нагревании или стоянии.
К 1 мл исследуемого вещества прибавляют 5 мл реактива Лукаса. Пробирку закрывают пробкой, энергично встряхивают и оставляют стоять на 5 мин. Третичные спирты при этом через 2-3 минуты образуют хлористый алкил, оседающий в виде нерастворимых в воде капель. Вторичные спирты дают помутнение раствора, а выделение галогенпроизводного наступает лишь 10 минут. Первичные спирты образуют гомогенный раствор, выделения хлоропроизводного не наблюдается. К 1 мл исследуемого вещества приливают 3 мл конц. соляной кислоты. Смесь сильно встряхивают и оставляют стоять на 3-5 мин. Третичные спирты при этом образуют нерастворимый в кислоте галоидный алкил. Первичные и вторичные спирты в этих условиях заметно не реагирует. Эта реакция позволяет отличить третичные спирты от вторичных. Многоатомные спирты. Реакция с гидроксидом меди (II). В двух-, трех– и многоатомных спиртах, содержащих 1,2-диольный фрагмент, в отличие от одноатомных спиртов растворяется свежеприготовленный гидроксид меди (II), с образованием темно–синего раствора комплексных солей соответствующих производных (гликолятов, глицератов). В пробирку наливают несколько капель (0,3-0,5 мл) 3 %-ного раствора сульфата меди, а затем 1 мл 10 %-ного раствора NaOH. Выпадает студенистый голубой осадок гидроксида меди (II). Растворение осадка при добавлении 1 мл исследуемого вещества и изменение цвета раствора до темно-синего подтверждает присутствие многоатомного спирта с гидроксильными группами, расположенными у соседних атомов углерода.
Фенолы Реакция с хлоридом железа (III). Фенолы дают с хлоридом железа(III) интенсивно окрашенные комплексные соли. Обычно появляется глубокая синяя или фиолетовая окраска, некоторые фенолы дают зеленое или красное окрашивание, оно ярче проявляется в воде или хлороформе и хуже в спирте. В пробирку помещают несколько кристаллов исследуемого вещества в 2 мл воды или хлороформа, затем добавляют при встряхивании 1-3 капли 3 %-ного раствора хлорида железа (III).В присутствии фенола появляется интенсивная фиолетовая или синяя окраска. Реакция с бромной водой. Фенолы со свободными орто- и пара- положениями в бензольном ядре легко обесцвечивают бромную воду, при этом получается осадок 2,4,6-трибромфенола.
Небольшое количество исследуемого вещества встряхивают с 1 мл воды, затем прибавляют по каплям бромную воду. Происходит быстрое обесцвечивание раствора и выпадение белого осадка.
Карбонильные соединения
В отличие от кетонов альдегиды легко окисляются. На этом свойстве основано открытие альдегидов. Реакция серебряного зеркала. Все альдегиды легко восстанавливают аммиачный раствор оксида серебра. Кетоны этой реакции не дают.
В хорошо вымытой пробирке смешивают 1 мл раствора нитрата серебра с 1 мл 25 %-ного раствора аммиака. Выпавший первоначально осадок гидроксида серебра быстро растворяется в избытке аммиака. К полученному раствору прибавляют несколько капель спиртового раствора анализируемого вещества. Пробирку помещают на водяную баню и нагревают при 50-60 0C 10-15 минут. Если на стенках пробирки выделяется блестящий налет металлического серебра, то это свидетельствует о наличии альдегидной группы в исследуемом образце. Следует отметить, что эту реакцию могут давать также и другие легко окисляющиеся соединения: многоатомные фенолы, 1,3-дикетоны и др. Реакция с гидросульфитом натрия. Альдегиды, алифатические метилкетоны и алициклические кетоны при взаимодействии с гидросульфитом натрия образуют хорошо кристаллизующиеся сульфитные соединения:
В пробирку помещают 0,2 г (или 2 мл) исследуемого вещества, приливают 1 мл этилового спирта и 1 мл насыщенного раствора гидросульфита натрия. Пробирку закрывают пробкой и сильно встряхивают. Выпадение кристаллического осадка свидетельствует о наличии карбонильного соединения. При отрицательных пробах на специфические реакции альдегидов, выпавший кристаллический осадок гидросульфитного соединения указывает на присутствие метилкетона или циклического кетона.
|