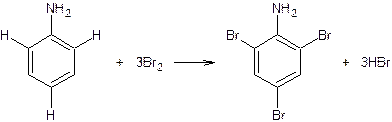Бромирование анилина
К 5 мл воды приливают 2-3 капли анилина и смесь сильно встряхивают. К полученной эмульсии по каплям прибавляют бромную воду. Смесь обесцвечивается, и выпадает белый осадок триброманилина. Введение в ароматическое кольцо аминогруппы резко повышает подвижность атомов водорода при атомах углерода бензольного кольца, поэтому анилин очень легко бромируется даже в разбавленном водном растворе с образованием малорастворимого в воде 2,4,6-триброманилина:
В результате бромирования основность анилина понижается, и триброманилин почти нерастворим в разбавленных кислотах.
Окисление анилина К 1мл анилиновой воды добавляют 2-3 капли раствора бихромата калия и 0,5 мл разбавленной серной кислоты. Жидкость окрашивается в интенсивный темно – зеленый цвет, переходящий в синий, а затем в черный. Окисление анилина протекает очень легко, и в зависимости от условий и характера окислителя образуются различные соединения: азобензол, азоксибензол, нитробензол, бензохинон и т.д. В условиях описанного опыта анилин при окислении дает различные сложные окрашенные соединения, содержащие хиноидную группу.
Продукт окисления «черный анилин» очень стоек к кислотам и щелочам, его применяют в качестве красителя.
Рекомендуемая литература к лабораторным работам 5. Практикум по органической химии. Под ред. Зефирова Н.С. М., Бином, 2010. 6. Органикум. М.: Мир. 1992. Т. 1,2. 7. Титце Л., Айхер Т. Препаративная органическая химия. М.: Мир. 1999. 8. Гордон А., Форд Р. Спутник химика. М.: Мир. 1976.
|