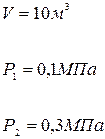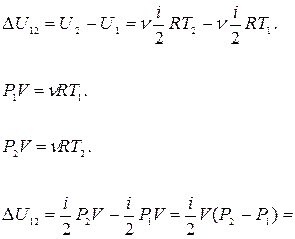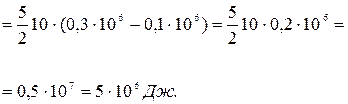Внутреннюю энергию 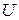 газа определяют как сумму кинетической энергии теплового движения молекул и потенциальной энергии межмолекулярного взаимодействия.
газа определяют как сумму кинетической энергии теплового движения молекул и потенциальной энергии межмолекулярного взаимодействия.
Получим выражение для внутренней энергии идеального газа. В идеальном газе пренебрегают силами межмолекулярного взаимодействия. Поэтому внутренняя энергия идеального газа равна кинетической энергии его молекул.
Расчет дает, что средняя кинетическая энергия молекул

(16. 1)
где 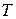 - температура газа,
- температура газа,  - постоянная Больцмана
- постоянная Больцмана
 , где
, где  - число Авогадро - число молекул в одном моле газа),
- число Авогадро - число молекул в одном моле газа), 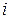 - число степеней свободы - число независымых координат, с помощью, которых может быть задано положение молекул в пространстве. Для определения положения в пространстве одноатомной молекулы достаточно трех координат
- число степеней свободы - число независымых координат, с помощью, которых может быть задано положение молекул в пространстве. Для определения положения в пространстве одноатомной молекулы достаточно трех координат  . Следовательно, для одноатомной молекулы
. Следовательно, для одноатомной молекулы  . Для определения положения в пространстве двухатомной молекулы достаточно трех координат
. Для определения положения в пространстве двухатомной молекулы достаточно трех координат  центра молекулы и двух значений углов
центра молекулы и двух значений углов 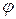 и
и  фиксирующих направление оси молекулы. Следовательно, для двухатомной молекулы
фиксирующих направление оси молекулы. Следовательно, для двухатомной молекулы 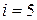 . для определения положения трехатомной и более молекулы в пространстве достаточно трех координат
. для определения положения трехатомной и более молекулы в пространстве достаточно трех координат  центра молекулы и трех значений углов
центра молекулы и трех значений углов 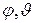 и
и 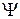 , фиксирующих направление оси молекулы. Следовательно, для трехатомной и многоатомной молекулы
, фиксирующих направление оси молекулы. Следовательно, для трехатомной и многоатомной молекулы 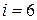 .
.
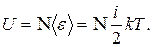
(16. 2)
Учитывая, что
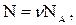
можем написать
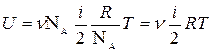
(16. 3)
Отметим, что внутренняя энергия является функцией состояния. Это означает, например, что при переходе газа из состояния 1 (с температурой 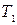 ) в состояние 2 (с температурой
) в состояние 2 (с температурой  ) приращение внутренней энергии
) приращение внутренней энергии 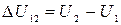 , т. е. не зависит от способа перехода газа из состояния 1 в состояния 2, а определяется только разностью значений внутренней энергии газа в состояния 1 и 2.
, т. е. не зависит от способа перехода газа из состояния 1 в состояния 2, а определяется только разностью значений внутренней энергии газа в состояния 1 и 2.
Пример 16. 1 Водород, находящийся при нормальных условиях в закрытом сосуде объемом  , охладили на
, охладили на 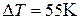 . Найти приращение внутренней энергии газа.
. Найти приращение внутренней энергии газа.
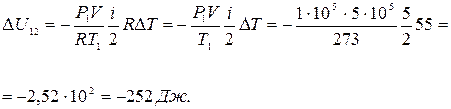
Ответ: 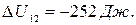
Пример 16. 2. Водород занимает объем 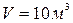 при давлении
при давлении  Его нагрели при постоянном объеме до давления
Его нагрели при постоянном объеме до давления 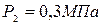 .Определить приращение
.Определить приращение 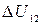 внутренней энергии газа.
внутренней энергии газа.
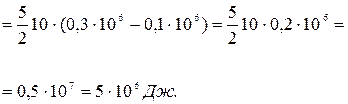
Ответ: 

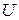 газа определяют как сумму кинетической энергии теплового движения молекул и потенциальной энергии межмолекулярного взаимодействия.
газа определяют как сумму кинетической энергии теплового движения молекул и потенциальной энергии межмолекулярного взаимодействия.
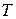 - температура газа,
- температура газа,  - постоянная Больцмана
- постоянная Больцмана , где
, где  - число Авогадро - число молекул в одном моле газа),
- число Авогадро - число молекул в одном моле газа), 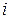 - число степеней свободы - число независымых координат, с помощью, которых может быть задано положение молекул в пространстве. Для определения положения в пространстве одноатомной молекулы достаточно трех координат
- число степеней свободы - число независымых координат, с помощью, которых может быть задано положение молекул в пространстве. Для определения положения в пространстве одноатомной молекулы достаточно трех координат  . Следовательно, для одноатомной молекулы
. Следовательно, для одноатомной молекулы  . Для определения положения в пространстве двухатомной молекулы достаточно трех координат
. Для определения положения в пространстве двухатомной молекулы достаточно трех координат 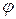 и
и  фиксирующих направление оси молекулы. Следовательно, для двухатомной молекулы
фиксирующих направление оси молекулы. Следовательно, для двухатомной молекулы 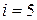 . для определения положения трехатомной и более молекулы в пространстве достаточно трех координат
. для определения положения трехатомной и более молекулы в пространстве достаточно трех координат 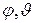 и
и 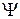 , фиксирующих направление оси молекулы. Следовательно, для трехатомной и многоатомной молекулы
, фиксирующих направление оси молекулы. Следовательно, для трехатомной и многоатомной молекулы 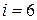 .
.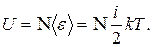
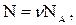
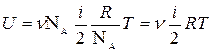
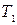 ) в состояние 2 (с температурой
) в состояние 2 (с температурой  ) приращение внутренней энергии
) приращение внутренней энергии 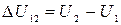 , т. е. не зависит от способа перехода газа из состояния 1 в состояния 2, а определяется только разностью значений внутренней энергии газа в состояния 1 и 2.
, т. е. не зависит от способа перехода газа из состояния 1 в состояния 2, а определяется только разностью значений внутренней энергии газа в состояния 1 и 2. , охладили на
, охладили на 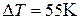 . Найти приращение внутренней энергии газа.
. Найти приращение внутренней энергии газа.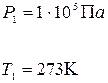

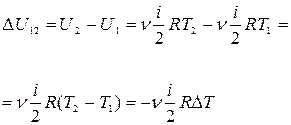
 >
>  .
.
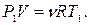
 .
.
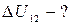
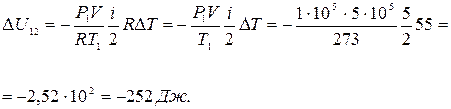
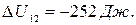
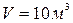 при давлении
при давлении  Его нагрели при постоянном объеме до давления
Его нагрели при постоянном объеме до давления 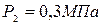 .Определить приращение
.Определить приращение 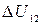 внутренней энергии газа.
внутренней энергии газа.