Главное в главе 1
Уравнение состояния идеального газа (часто называемое в России уравнением Менделеева–Клапейрона)
хорошо известно из школьного курса физики. Рассмотрены изотермический, изобарный, изохорный процессы в идеальном газе. Результаты приведены в табл. 6.1. Изложена теория осмотического давления. С использованием основных положений молекулярно-кинетической теории (МКТ): 1) вещество состоит из частиц; 2) эти частицы непрерывно и хаотически движутся; 3) частицы взаимодействуют между собой, рассмотрены основы строения твердых, жидких и газообразных тел. Для идеального газа на основе положений МКТ построено основное уравнение МКТ идеального газа:
Сравнение приведенных двух уравнений, описывающих один и тот же объект — идеальный газ, позволяет связать макроскопические характеристики газа с микроскопическими характеристиками отдельной молекулы. Средняя кинетическая энергия молекулы связывается с температурой газа
где k = R / NА называется постоянной Больцмана.
|

 (1.21)
(1.21)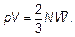 (1.47)
(1.47) (1.48)
(1.48)


