И термодинамический методы исследования
Глава 5. Физические основы молекулярной физики и Термодинамики
Молекулярная физика – это раздел физики, в котором изучаются строение и свойства вещества, исходя из молекулярно-кинетических представлений. Эти представления включают в себя следующие положения: - любое тело (твердое, жидкое, газообразное) состоит из большого числа частиц - молекул или атомов; - молекулы находятся в непрерывном хаотическом движении, не имеющим какого-либо преимущественного направления; - взаимодействие между собой зависит от типа молекул и расстояний между ними (разные агрегатные состояния). Обоснованность названных положений является полностью доказанной в настоящее время.
Статистический (молекулярно-кинетический) и термодинамический методы исследования В молекулярной физике и термодинамике используют 2 метода изучения свойств и строения вещества: молекулярно-кинетический или статистический и термодинамический. В молекулярно-кинетическом (статистическом) методе законы протекания различных процессов в макротелах устанавливаются на основании изучения их молекулярной структуры и механизма взаимодействия отдельных молекул между собой. Физические характеристики отдельных молекул - масса, скорость, концентрация, энергия и др. - после статистической обработки увязываются с макрохарактеристиками тел – давлением, температурой, плотностью и др. Термодинамический метод изучает макроскопические свойства тел, не интересуясь их микроскопической структурой. Не вводя в рассмотрение молекулы и атомы, термодинамика позволяет сделать целый ряд выводов относительно протекания процессов посредством измерения параметров - давления, температуры, плотности и др. В основе термодинамики лежат законы (начала) термодинамики. Состояние тела или системы тел определяется совокупностью его параметров в данный момент времени. Величины, характеризующие состояние системы тел, называются параметрами состояния. Параметрами термодинамической системы являются: ρ – плотность – отношение массы к объему. При однородном ее распределении по объему
P - давление – отношение силы к площади Т- температура – термодинамическая величина, характеризующая состояние термодинамического равновесия системы (степень нагретости -характеристика, не дающая полного определения температуры). Единица измерения в СИ- Кельвин. Существует несколько шкал для измерения температуры. В нашей стране используют две шкалы – Цельсия и Кельвина. За единицу измерения температуры принята 1/100 разности температур таяния льда и кипения воды при нормальных условиях и называется эта единица градусом Цельсия (0С) при использовании шкалы Цельсия, или Кельвином при использовании шкалы Кельвина. Начало шкалы Кельвина (0 Кельвинов) сдвинуто от 00 С в отрицательную область на 273,15 единиц. Поэтому связь между температурами t по Цельсию и Т по Кельвину имеет вид Т= t + 273,15 m - Масса молекулы выражается через молекулярный вес – отношение молекулярной массы данного вещества к 1/12 массы атома изотопа углерода 12С, масса которого принята равной 12 единицам, а масса одной единицы равна 1,66 ∙ 10-27 кг. Молекулярный и атомный веса - величины безразмерные. Масса вещества в кг (молярная масса), численно равная молекулярному весу вещества называется киломолем и обозначается М. Масса вещества в г, численно равная молекулярному весу называется молем и также обозначается М. Измеряются в кг/кмоль, г/моль или кг/моль.
|

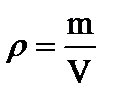 [кг/м3], при неоднородном распределении
[кг/м3], при неоднородном распределении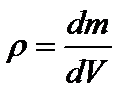
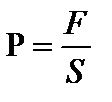 [Па].
[Па].


