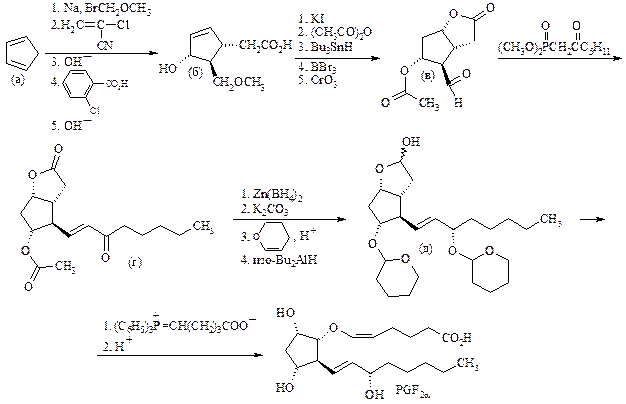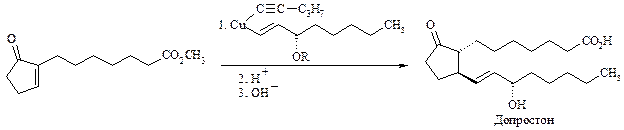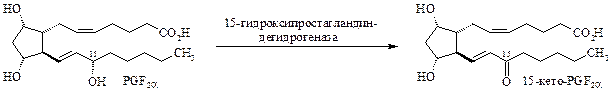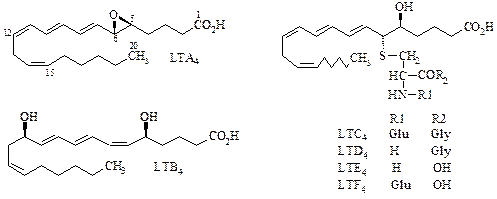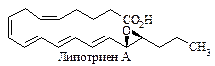Простагландины и тромбоксаны
Простагландины и тромбоксаны – биорегуляторы липидной природы, представляющие собой оксигенированные производные полиеновых жирных кислот, содержащих в углеводородной цепи пяти- или шестичленные циклы. Они обнаружены практически во всех тканях млекопитающих и обладают исключительно высокой и разносторонней физиологической активностью. Как правило, простагландины не накапливаются в тканях и органах в свободном виде, а синтезируются внутриклеточными ферментами в ответ на биологический стимул и оказывают свое действие глазным образом в непосредственной близости от места образования. В 30-х годах нашего столетия гинеколог Р. Курцрок и фармаколог Ч. Либ (США) обнаружили, что в семенной жидкости человека присутствует фактор, способный вызвать сильное сокращение или расслабление гладких мышц матки, а несколько позже Ульф фон Эйлер (Швеция) и М. Гольдблатт (Великобритания) нашли, что при инъекции животным он не только стимулирует гладкую мускулатуру, но и влияет на артериальное давление. Исследовав химическую природу нового фактора, Эйлер отнес его к классу липидов и предложил название «простагландин» (PG), так как считал, что он образуется в предстательной железе (от лат. prostata). Успехи в исследовании структуры простагландинов во многом связаны с именем шведского ученого Бергстрёма. Благодаря использованию таких методов, как противоточное распределение, хроматография на бумаге, газовая хроматография и масс-спектрометрия, ему уже к концу 50-х годов удалось выделить индивидуальные соединения, а в 1962 г установить строение первых трех простагландинов, которое было подтверждено в 1963 г С. Абрахамсоном с помощью рентгеноструктурного анализа. В 1965 г. группами С. Бергстрёма (Швеция) и Д. ван Дорпа (Нидерланды) было установлено, что простагландины образуются в результате ферментативного окисления арахидоновой кислоты. Благодаря этому открытию простагландины, препаративно получаемые путем биосинтеза, стали легкодоступны для биологических испытаний, что позволило изучить разнообразные аспекты их физиологического действия. Одновременно начались работы по химическому синтезу простагландинов, значительный вклад в которые внес Э. Кори (США). В 1976 г. группами Дж. Вейна (Великобритания) и Б. Самуэльсона (Швеция) были обнаружены новые метаболиты арахидоновой кислоты – простациклин (РGI2) и тромбоксан А2(ТХА2), также обладающие высокой биологической активностью. В настоящее время известно 10 типов простагландинов (А, В, С, D, Е, F, G, Н, I, J) и 2 типа тромбоксанов (А и В). Все простагландины имеют циклопентановое кольцо, несущее кислородсодержащие функциональные группы. Для тромбоксанов характерен тетрагидропирановый цикл. Простагландины и тромбоксаны – карбоновые кислоты, содержащие в положении 15 аллильную гидроксильную группу. В зависимости от числа двойных связей в молекуле они подразделяются на три серии, обозначаемые подстрочными индексами 1, 2 и 3. Для простагландинов F в подстрочном индексе дополнительно указывается конфигурация (a или b) гидроксильной группы при С-9 (рис. 365).
Рис.365 Строение важнейших простагландинов тромбоксанов. Простагландины и тромбоксаны – весьма реакционноспособные соединения. Некоторые из них, например PGA2, PGH2, TXA2, реагируют с компонентами плазмы крови, в частности с альбумином, теряя при этом биологическую активность. Напротив, РGI2 стабилизируется альбумином. Химическая нестабильность простагландинов и тромбоксанов связана с наличием в них аллильной гидроксильной группы, которая сравнительно легко эпимеризуется, окисляется или отщепляется, что приводит к потере активности содержащих простагландины лекарственных препаратов. Синтез простагландинов с природной конфигурацией всех хиральных центров молекулы является сложной задачей. К настоящему времени разработаны стереоспецифические схемы синтеза, приводящие к оптически активным простагландинам, например осуществленный Элайсом Кори синтез PGF2a, имеющего 5 хиральных центров.
Из циклопентадиена (а) конструируется циклическая часть молекулы, которая содержит функциональные заместители, характерные для PGF2a, и реакционноспособные группы, необходимые для наращивания боковых цепей. При этом строго контролируется конфигурация создаваемых хиральных центров. Образовавшиеся антиподы разделяются кристаллизацией с (+)-эфедрином. Синтон (б) (т.е. ключевое промежуточное соединение, в котором созданы реакционноспособные группировки, необходимые для последующих химических превращений) с природной конфигурацией хиральных центров превращается в альдегидолактон (в), и по реакции Виттига в него вводится одна из двух алифатических цепей с образованием кетона (г). В лактоне (д) с 15S-конфигурацией гидроксильной группы по реакции Виттига достраивается вторая цепь, и затем удаляются защитные группы. Ключевая стадия другого подхода к синтезу простагландинов – конденсация циклопентенового синтона (а), содержащего готовую верхнюю цепь, с медь-органическим реагентом, вводящим нижнюю цепь. По этой схеме в СССР синтезировался препарат «Допростон», представляющий собой стабильный аналог PGE1.
Таким образом, полный химический синтез не только позволяет подтвердить структуру простагландинов и делает их коммерчески доступными, но также открывает широкие возможности для получения аналогов. Простагландины и тромбоксаны синтезируются в организме животных и человека из полиненасыщенных жирных кислот с длиной цепи 20 углеродных атомов (эйкозаполиеновых). Биосинтетический предшественник важнейших простагландинов – арахидоновая кислота, она входит в состав фосфолипидов и в свободном виде практически не встречается. Из 20:3 w6-, 20:4 w6- и 20:5 w3-кислот образуются РG1, PG2, и PG3, соответственно.
cхема 1 Минимальный структурный фрагмент – система w6,9,12, преимущественно С20 – кислота; биосинтез осуществляется через эндо-пероксиды (схема 1), которые являются предшественниками как простагландинов, так и тромбоксанов. Биосинтез простагландинов начинается с гидролиза фосфолипидов, содержащих арахидоновую кислоту, под действием мембранной фосфолипазы А2. Фермент циклооксигеназа катализирует далее стереоспецифическое присоединение пероксидных радикалов по положениям 11 и 15 арахидоновой кислоты с образованием 9,11-пероксидного мостика и циклизацией по положениям 8 и 12. Образующийся крайне неустойчивый PGG2 восстанавливается пероксидазой до более стабильного PGH2. Циклооксигеназную и пероксидазную активность проявляет, по-видимому, один и тот же фермент – PGН2-синтетаза.
Простагландины и тромбоксаны участвуют в регуляции многих функций организма. В некоторых случаях они действуют как синергисты (так, PGI2, PGE, и PGD2 ингибируют агрегацию тромбоцитов), в других – являются антагонистами (PGI2 расслабляет артерии, а ТХА2 сокращает). Простагландины обеспечивают нормальное течение физиологических процессов. Так, гемоcтаз зависит от соотношения между ТХА2 и РGI2. Простагландины Е1 и Е2 важны для нормального функционирования сердечно-сосудистой системы плода во время беременности. PGE1 и PGE2 подавляют секрецию желудочного сока и, по-видимому, служат природными цитопротекторами. Простагландины регулируют тонус гладких мышц, в том числе сосудов, играют важную роль в поддержании иммунного статуса организма и могут блокировать функции некоторых иммунокомпетентных клеток. Все, что известно сейчас о простагландинах и тромбоксанах, позволяет считать их «сверхгормонами». Это подтверждается весьма высокой активностью, зарегистрированной в опытах in vitro. Простагландины вызывают высокоспецифичные эффекты в концентрациях 10-13–10-15 М, что на несколько порядков ниже их содержания в биологических жидкостях. Способность простагландинов оказывать действие в столь низких концентрациях дает основание рассматривать их не просто как локальные биорегуляторы, но и как циркулирующие гормоны, необходимые, вероятно, для регуляции функций всего организма или его отдельных органов и тканей. Поиск новых аналогов простагландинов с улучшенными фармакологическими свойствами – одна из важнейших задач биоорганической химии, поскольку простагландины все шире используются как эффективные препараты в медицине и сельском хозяйстве. Для практического применения необходимы химически и метаболически устойчивые аналоги простагландинов. Например, от действия 15-гидрокси-простагландин-дегидрогеназы – фермента, инициирующего метаболическую инактивацию простагландинов,
хорошую защиту дает введение заместителей (CH3 или F) в положения 15 или 16, а также замена концевого алкильного остатка на феноксигруппу:
Сегодня для практики доступны препараты не только природных простагландинов: РGЕ1 (алпростадил), PGE2 (простенон), PGF2a (энзапрост), PGI2 (эпопростенол натрий), но и их синтетических аналогов (сульпростон, арбапростил, эструмат, илопрост и т. д.).
Лейкотриены Лейкотриены объединяют группу липидных биорегуляторов, образующихся из эйкозаполиеновых кислот в результате окисления липоксигеназами. Происхождение термина «лейкотриен» (LT) связано с первоначальным обнаружением этих соединений в лейкоцитах (1979), а также с тем, что в их молекулах имеется характерная система из трех сопряженных двойных связей. Подобно простагландинам, лейкотриены обладают высокой физиологической активностью и синтезируются в организме в ответ на определенный стимул. Лейкотриены – важные медиаторы воспалительных реакций и анафилаксии (болезненной аллергической реакции немедленного типа, возникающей в ответ на введение аллергена). Различают 6 типов лейкотриенов (А, В, С, D, E, F), причем четыре из них (С–F) содержат остаток цистеина или цистеинилпептида.
Кроме того, недавно были обнаружены изомеры лейкотриенов, содержащие заместители в положениях 14, 15. Для них предложено название «липотриены».
Наконец, в 1984 г. открыта новая серия метаболитов арахидоновой кислоты в лейкоцитах человека; эти соединения, названные липоксинами (LX), имеют в своей структуре систему из четырех сопряженных двойных связей.
Как и многие другие биорегуляторы липидной природы, лейкотриены долгое время оставались химически неидентифицированными. В (1938 г. В. Фельдберг и Г. Келлауэй заметили, что при перфузии изолированного легкого морской свинки раствором, содержащим яд кобры, образуется какое-то вещество, вызывающее сокращение тонкой кишки. Этот эффект, в отличие от действия гистамина, развивается во времени значительно медленнее. Отсюда произошло название «медленно реагирующее вещество» (от англ. slow-reacting substance, SRS). В начале 50-х годов В. Брохлест установил, что во время анафилаксии образуется сходное вещество – SRS-A. В 60-е годы удалось выяснить, что SRS-A – полярный липид, отличающийся от простагландинов; однако из-за недостаточного количества материала для исследования его структура осталась невыясненной и было лишь определено, что SRS-A имеет молекулярную массу около 500 и содержит серу. Примерно в то же время Б. Самуэльсон. изучавший продукты метаболизма арахидоновой кислоты в полиморфоядерных лейкоцитах кролика, обнаружил новое дигидроксипроизводное. содержащее триеновый хромофор. Далее удалось показать, что это производное, названное позднее лейкотриеном В4, образуется из другого, менее стабильного, но биологически весьма активного вещества. В результате работы исследовательских групп Б. Самуэльсона и Э. Кори была установлена структура LTA4 – нестабильного промежуточного соединения в биосинтезе LTB4 и осуществлен его химический синтез, который позволил сделать окончательный выбор между несколькими стереомерными структурами. В 1979 г. Б. Самуэльсон сообщил, что SRS-A представляет собой смесь пептидных лейкотриенов. образующихся при реакции LTA4 с цистеином и цистеинсодержащими пептидами. Структура пептидных лейкотриенов (LTC–LTF) была подтверждена стереоспецифическим синтезом (Э. Кори и Дж. Рокач). Лейкотриены и родственные им соединения стали доступны для широких биологических испытаний только после разработки метода их химического синтеза. Пептидные лейкотриены получают из синтетического LTA4 и соответствующего пептида, т. е. по схеме, аналогичной биосинтезу этих соединений; сам LTA4 можно получить как полным химическим синтезом, так и путем химической трансформации арахидоновой кислоты. По биологической активности лейкотриены значительно превосходят другие известные биорегуляторы, например гистамин. Они играют существенную роль в развитии различных патологических состояний. Миотропные пептидиые лейкотриены (LTC4 и LTD4) влияют на процесс дыхания. Лейкотриены активно сокращают гладкие мышцы желудочно-кишечного тракта, действуют и на сердце, вызывая сильное сокращение коронарных сосудов; возможно, они участвуют в развитии ишемии миокарда. Наряду с липоксинами и простагландинами лейкотриены служат также важными регуляторами иммунной системы. Таким образом, существуют два главных пути метаболизма арахидоновой кислоты: циклооксигеназный – до простагландинов и тромбоксанов и липоксигеназный – до лейкотриенов и липоксинов. Вместе с другими реакциями окисления они входят в общую сеть процессов метаболизма, называемую «каскадом арахидоновой кислоты» (рис. 367).
Как правило, в клетках и тканях экспрессированы не все ферменты каскада, поэтому состав метаболитов арахидоновой кислоты может служить характеристикой функционального состояния клеток. Активность многих широко применяемых лекарственных препаратов системного типа (например, аспирина) связана с их воздействием на одну или несколько ступеней этого каскада.
|