Снижение пропускной способности трубопроводов при эксплуатации ГиГКМ.
Г-овые гидраты представляют собой кристаллические соед-я, образуемые ассоциируемыми мол-лами воды и Г. На вид снег или лед. Все применяемые методы борьбы с г/о-нием основаны на изменении энергетических соотношений мол-л Г (г/о-теля) и воды. На практике Наиболее широко для борьбы применяют: – осушка Г-ового потока методами сорбции и НТС;– ввод в Г-овый поток ингибиторов; – поддержание t-ры Г > t-ры г/о-ния;–поддержание Р Г < Р г/о-ния. Парафины Пар-ны могут откладываться за счет: 1) возникновения и роста кристаллов пар-на на пов-ти трубы; 2) сцепления с поверхностью образовавшихся в потоке частиц твердой фазы. t-раоказывает наибольшее влияние на равновесие ж-ть – твердая фаза. Растворимость пар-на сильно зависит от t-ры и уменьшается с увеличением t-ры плавления пар-новых фракций. Применение присадок решает проблему на всем пути сырья от скв-ны до перерабатывающего завода. Несмотря на применение узла приготовления раствора и высокую стоимость присадок, они наиболее выгодны и эффективны. Широкое применение на нек-х мест-ях нашли реагенты – растворители (горячая нефть, Г-овый к-т, ароматические углеводороды, бутил-бензольная фракция (ББФ), спирты керосин). Солеотложения Поступлении пл-ой воды (сильно минерализованной) в скв-ны, вызывая серьезные затруднения в эксплуатации. В пл-ой воде распространены: NaCl, MgCl, CaCl, карбонаты (СаСО3, MgCO3) и бикорбанаты, сульфаты (СаSO4), окислы и гидроокиси железа. Эти соли выпадают из раствора при изменении т/д-х усл-й. Отложение солей наблюдается в фонтанной арматуре, шлейфах, сеп-рах на УКПГ. Отложения солей приводят к частым остановкам для ремонта и замены оборудования. Методы борьбы с отложением солей подразделяются на физические и химические. Физические методы основаны на применении магнитных, электрических (высокочастотных) и акустических (распространение ультразвуковых волн) полей. Химические методы. К основным химическим методам обработки воды относятся: умягчение воды посредством ионного обмена и применение химических реагентов – ингибиторов солеотложения, получило наибольшее распространение для борьбы с солеотложениями. Наиболее перспективными являются фосфорорганических комплексоны из класса аминоалкиленфосфоновых кислот. 21. Зависимость функции коэффициента Джоуля-Томсона от приведенных давления и температуры. Номограмма для определения интегрального дроссель-эффекта Джоуля-Томсона. Поmi=(Тк/Рк)×[Рк×mi×Cp/Tк]/(Сро+DСР) можно вычислить коэффициент Дж.-Томсона при этом обобщенная функция Рк×mi×Cp/Tк в зав-ти от прив. параметров определяется по графику рис. 1. Среднее отклонение, вычисленных по нашему методу коэффициентов Дж.-Томсона. для чистых компонентов и смесей от опытных данных составляют 7 %. При пост. Р-х и t-рах коэф. Дж.-Томсона. для сухого у/в-го газа имеет большую величину для газа с большой молекулярной массой. При промысловых расчетах, связанных с дросселированием газа, обычно пользуются интегральным дроссель-эффектом, который определяется как произведение средних значений: дифференциального дроссель-эффекта на изменение давления. Для аналитического определения дроссель эффекта при изменении давления от Р1 до Р2, необходимо проинтегрировать величину:
Для газа, подчиняющегося уравнению Ван-дер-Ваальса, Чарный получил из (23) след. Выражение Т1–Т2+2×а×ln[(2×a–T1)/(2×a–T2)]=A×b×(P1–P2)/CP (24) где Т1, Т2 – начальная и конечная температура газа; Р1, Р2 – начальное и конечное давления газа; СР – уд. теплоемкость газа. a=27×R2×Tкр2/(64×Ркр) (25) b=R×Tк/(8×Рк) (26) (26) можно преобразовать к виду для расчета интегрального дроссель эффекта. DТ=Т1–Т2=А×R×Tк/(8×СР)(1/t¢1–1)×(p1–p2) (27) где: p¢1=p¢/Тинв (28) p1=Р1/Ркр (29) p2=Р2/Ркр (30) Тинв=27/(4×Ткр) (31) формулу 27 можно преобразовать к след виду: DТ=5,569×(1/t¢1–1)(p1–p2) (32) анные, полученные по (27) и (32) совпадают с экспериментальными, и данными. (32) можно использовать для расчета интегрального эффекта ПГ с содержанием газа >90 %. Уменьшение температуры природного газа при данном изменении еа штуцере и известном давлении газа можно определить по рис. 2. При интегральных расчетах температуру газа в процессе дросселирования можно определить энтальпийным диаграммам, т.е. диаграмма состояния, которые для каждого индивидуального компонента газа строятся экспериментальным данным. Чаще всего параметры процесса дросселирования определяются по диаграммам состояния для чистого газа.
|

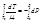 (23)
(23)


